сколько живут после удаления меланом кожи, иссечение меланомы
Хирургия — основной вид лечения меланомы. Большинству пациентов, после того как диагноз подтвержден при помощи биопсии, показано хирургическое лечение. Во время операции врач стремится удалить из организма пациента всю опухолевую ткань, чтобы не допустить рецидива в будущем.
Прибегают к разным видам хирургического вмешательства, в зависимости от стадии, размеров и расположения меланомы.
Какие виды операций выполняют при меланоме?
Чаще всего выполняют широкое иссечение меланомы. Хирург удаляет опухоль и некоторое количество здоровой ткани вокруг неё. Здоровая ткань вокруг опухоли называется краем резекции. После иссечения врач должен обязательно отправить то, что удалил, в лабораторию. Край резекции изучают под микроскопом на предмет наличия опухолевых клеток:
- негативный результат означает, что раковых клеток в крае резекции нет, меланома удалена полностью;
- позитивный результат говорит о том, что раковые клетки присутствуют в образце, опухоль не удалена, нужна повторная операция.

Размеры края резекции измеряются в сантиметрах и зависят от стадии меланомы:
| Стадия меланомы T | Толщина (глубина прорастания) | Размер края резекции |
| Tis | «Рак на месте»: опухоль не прорастает в дерму | 0,5–1 см |
| T1 | Менее 1 мм | 1 см |
| T2 | 1–2 мм | 1–2 см |
| T3 | 2–4 мм | 2 см |
| T4 | Более 4 мм | 2 см |
Также ширина края резекции зависит от того, на какой части тела находится меланома. Если опухоль расположена на лице, важен косметический эффект. Врач может захватить меньше здоровой кожи, но это повышает риск рецидива. Данный вопрос нужно заранее обсудить с хирургом.
Другие виды операций, которые выполняются при меланоме:- Биопсия сторожевого лимфоузла (сентинель-биопсия).
/iStock_24463523_LARGE-5809a6205f9b58564cf5ff19.jpg) Сторожевым называют ближайший к опухоли лимфатический узел. Он представляет собой первый рубеж, который предстоит преодолеть раковым клеткам, распространяющимся лимфогенным путем. Если опухоль проникла в него, есть вероятность, что она распространилась и в другие близлежащие лимфоузлы. Для того чтобы обнаружить сторожевой лимфатический узел, хирург вводит в ткани, окружающие меланому, специальный краситель. Лимфоузел, который первым прокрашивается, и является сторожевым. Его нужно удалить и отправить на исследование в лабораторию. Существует и более современный метод обнаружить сторожевой лимфоузел: вместо красителя в ткань вводят специальный слабый радиофармпрепарат и следят за его распространением при помощи гамма-камеры.
Сторожевым называют ближайший к опухоли лимфатический узел. Он представляет собой первый рубеж, который предстоит преодолеть раковым клеткам, распространяющимся лимфогенным путем. Если опухоль проникла в него, есть вероятность, что она распространилась и в другие близлежащие лимфоузлы. Для того чтобы обнаружить сторожевой лимфатический узел, хирург вводит в ткани, окружающие меланому, специальный краситель. Лимфоузел, который первым прокрашивается, и является сторожевым. Его нужно удалить и отправить на исследование в лабораторию. Существует и более современный метод обнаружить сторожевой лимфоузел: вместо красителя в ткань вводят специальный слабый радиофармпрепарат и следят за его распространением при помощи гамма-камеры. - Лимфодиссекция. Во время этой операции вместе с меланомой удаляют все регионарные лимфоузлы. Например, если опухоль находится на ноге, врач может удалить лимфоузлы в области паха. Лимфодиссекция может приводить к такому тяжелому осложнению как лимфедема — отек, вызванный нарушением оттока лимфы.
- Ампутация. Иногда, если опухолью поражена целая часть тела, например, палец, её приходится ампутировать.
Существует еще операция Мооса, но в настоящее время она критикуется многими врачами и применяется редко. Суть метода в том, что врач удаляет меланому тонкими слоями. Каждый слой осматривают под микроскопом. Как только раковые клетки перестают обнаруживаться, считается, что злокачественная ткань полностью удалена.
Хирургическая тактика в зависимости от стадии меланомы
Если меланома имеет толщину менее 0,75 мм, можно ограничиться широким иссечением без удаления лимфатических узлов. Такую операцию выполняют под местной анестезией.
При толщине меланомы 0,76 см и более нужно проводить сентинель-биопсию. Если раковые клетки в сторожевом лимфатическом узле не обнаружены, операцию заканчивают. Если же сторожевой лимфоузел поражен опухолевым процессом, диагностируют меланому III стадии и выполняют лимфодиссекцию. Регионарные лимфатические узлы удаляют под наркозом.
При метастатической меланоме (IV стадия) об излечении от рака речи не идет, но пациенту можно помочь. Активное паллиативное лечение помогает продлить жизнь и избавить от мучительных симптомов. Можно удалить хирургическим путем первичную опухоль, регионарные лимфатические узлы, метастазы в других органах. Однако даже если обнаружено всего 1–2 метастаза, скорее всего, есть и другие, просто они настолько малы, что пока незаметны.
Врачи «Евроонко» проводят комплексное лечение меланомы на любой стадии по современным стандартам. Помимо хирургических методов, мы используем современные химиопрепараты, таргетные препараты. На I и II стадиях от опухоли можно избавиться в 99% случаях. При некурабельной меланоме можно улучшить состояние и продлить жизнь. Для того чтобы получить наиболее эффективное и современное лечение, не обязательно ехать за границу. Звоните, мы знаем, как помочь.
Израильский научный медицинский центр Меланома Юнит в Москве
Стадирование меланомы
Стадирование меланомы или, иначе, определение стадии развития опухоли основывается на её толщине, размере, скорости распространения метастаз, изъявлении новообразования (как часто и сильно проявляется симптоматика), поражении лимфоузлов, а также других органов.
Для определения стадии необходимо провести комплексное обследование. Оно проводится следующим образом:
- Приём и осмотр пациента дерматологом-онкологом.
- Аппаратный дерматоскопический осмотр.
- Гистологический анализ.
- Биохимический анализ крови.
Осмотр пациента с применением диагностических методов, таких как: компьютерная томография (КТ), рентгенография, исследование при помощи ультразвука (УЗИ), магнитно-резонансная томография (МРТ).
Определить стадию развития меланомы крайне важно, так как это помогает назначить наиболее действенное лечение, применить нужный метод в борьбе со злокачественным новообразованием.
Методы определения стадий меланомы
В целом, основных методов определения стадий меланомы – два.
Клинический– основывается на осмотре пациента специалистом и полученных результатах биопсии (морфологическое исследование образца клеток).
Гистологический– основывается на микроскопическом методе исследования тканей, органов и систем организма, с применением биопсии и операционных методов. Гистологический анализ, как правило, показывает более высокую стадию развития злокачественного новообразования. Так, если биопсия показала, к примеру, 3-ю стадию меланомы, то гистологический анализ может показать уже 4-ю стадию развития рака кожи.
Гистологический анализ, как правило, показывает более высокую стадию развития злокачественного новообразования. Так, если биопсия показала, к примеру, 3-ю стадию меланомы, то гистологический анализ может показать уже 4-ю стадию развития рака кожи.
| Стадия меланомы | Характеристика распространения меланомы |
| 0 стадия | Tis, N0, M0– самая ранняя стадия. Эта стадия обозначает то, что новообразование не распространилось на нижний слой (дерму). Меланома находится в эпидермисе. |
| IA стадия | T1a, N0, M0– стадия меланомы 1A, злокачественное новообразование размером тоньше 1 мм. Эта стадия обозначает, что меланома не изъявлена. Скорость распространения метастаз – меньше 1/мм2. Меланома ещё не поразила лимфатические узлы или дистальные органы. |
| IB стадия | T1b или T2a, N0, M0– стадия меланомы 1B, злокачественное новообразование размером тоньше 1 мм. Меланома изъявлена, скорость распространения метастаз – меньше 1/мм2. |
| IIA стадия | T2b или T3a, N0, M0– стадия меланомы 2A. На этой стадии толщина меланомы может варьироваться от 1,01 до 2,0 мм, новообразование – изъявлено. Также толщина меланомы может быть от 2,01 до 4,00 мм, но новообразование – не изъявлено. Меланома ещё не поразила лимфатические узлы или дистальные органы. |
| IIB стадия | T3b или T4a, N0, M0– стадия меланомы 2B. На этой стадии толщина меланомы может быть от 2,01до 4,00, новообразование – изъявлено. Также толщина новообразования может быть больше 4,00мм, но оно – не изъявлено. В дистальных органах и лимфатических узлах меланома отсутствует. |
| IIC стадия | T4b, N0, M0– стадия меланомы 2C. На данной стадии толщина меланомы составляет 4 мм, она – изъявлена. |
| IIIA стадия | T1a до T4a, N1a или N2a, M0. На этой стадии толщина меланомы – любая, она – не изъявлена. Меланома уже распространилась на 1-3 лимфатическихузла, расположенных рядом с тем участком кожи, который является поражённым. Однако узлы ещё не увеличены. Меланома видна только при тщательном просмотре под микроскопом. Она ещё не распространилась на отдалённые участки. |
| IIIB стадия | T1b до T4b, N1a или N2a, M0. На этой стадии толщина меланомы также любая, но она – изъявлена. Меланома на данной стадии уже распространилась на 1-3 лимфатических узла, расположенных рядом с тем участком кожи, который является поражённым. Однако узлы ещё не увеличены. Меланома видна только при тщательном просмотре под микроскопом. Она ещё не распространилась на отдалённые участки. T1a до T4a, N1b или N2b, M0. Толщина меланомы – любая, она – не изъявлена. Меланома уже успела распространиться на 1-3 лимфатических узла, расположенных рядом с тем участком кожи, который является поражённым. T1a до T4a, N2c, M0. Толщина меланомы – любая, она – не изъявлена. Меланома уже успела распространиться на близлежащие небольшие участки кожи или, возможно, на лимфатические каналы, находящиеся рядом с новообразованием. Сами узлы, однако, не содержат меланомы. Меланома ещё не распространилась на отдалённые участки. |
| IIIC стадия | T1b до T4b, N1b или N2b, M0. Меланома на этой стадии изъявлена, её толщина может быть любого размера. Зона распространения меланомы в данном случае – 1-3 лимфатических узла, расположенных рядом с новообразованием, поразившем кожный покров. Наблюдается увеличение лимфатических узлов. На отдалённые участки меланома не распространилась. T1b до T4b, N2c, M0. Меланома также изъявлена, толщина – любая. В данном случае она распространяется на лимфатические каналы, находящиеся рядом с опухолью, и близлежащие участки кожи. Лимфатические узлы не поражены меланомой. Любые T, N3, M0. В данном случае меланома может быть изъявлена, а может – и нет, её толщина также может быть любой. Она уже распространяется на 4, а может, и больше скученных вместе лимфатических узла, находящихся рядом с местом поражения. Также может быть распространена на лимфатические каналы, проходящие рядом с новообразованием, и близлежащие участки кожи. Лимфатические узлы увеличены. Распространение на более отдалённые участки – отсутствует. |
| IV стадия | Любые T, любые N, M1(a, b, или c). На этой стадии меланома уже распространяется далеко за пределы того места на коже, где она проявилась. Через ближайшие лимфатические узлы она также распространяется на другие органы. Меланома может перекинуться на мозг, задеть печень и лёгкие. Она может поразить и отдалённые лимфатические узлы, и отдалённые участки кожи, и подкожные ткани. В данном случае не приходится рассматривать распространение меланомы на лимфатические узлы, расположенные рядом, а также её толщину.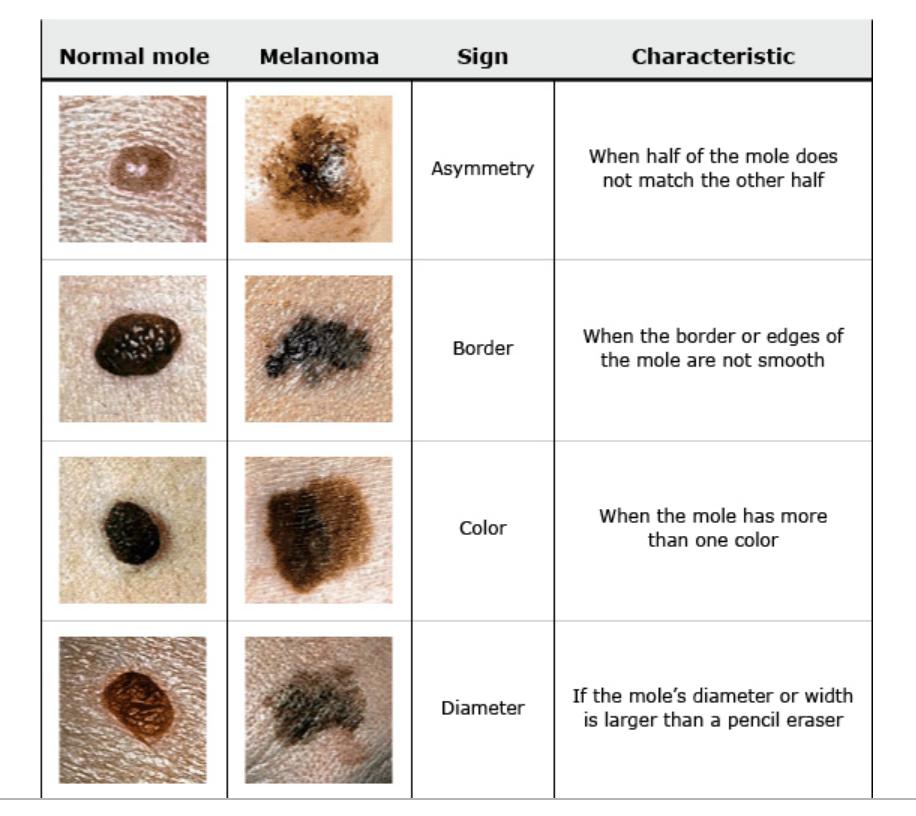 Но, обычно, она бывает весьма объёмной и поражает лимфатические узлы. Но, обычно, она бывает весьма объёмной и поражает лимфатические узлы. |
Меланома и её классификация
Выделяется несколько классификаций меланом, чтобы определить ту или иную стадию рака кожи. Это: классификация по Кларку, классификация по А. Бреслоу, классификация с использованием митотического индекса. Наиболее распространена классификация по системе TNM. Американское общество, занимающееся изучением рака – AJCC, явилось разработчиком данной системы классификации. TNMрасшифровывается как: Tumor– опухоль, LymphNode– лимфатический узел, Metastasis– метастазы. В этой аббревиатуре заложены ключевые позиции, призванные определить ту или иную степень развития меланомы.
T-категория
Этой категорией обозначается объём опухоли (её толщина). Измеряют её по системе Бреслоу. Учитывается и скорость развития метастаз – быстрота распространения на ткани и органы, отсутствие или наличие изъявлений меланомы – имеющиеся, например, повреждения или разрывы верхнего слоя кожи над местом расположения опухоли.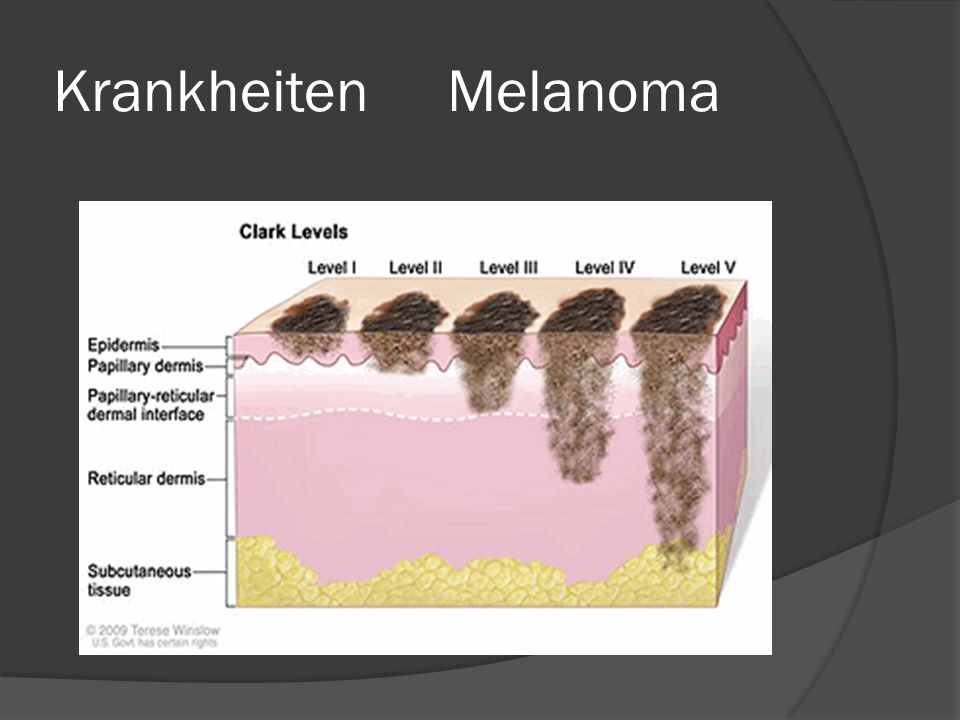 Сочетание T1a, к примеру, характеризует проявление меланомы на 1-й стадии, а вот сочетание T4b– является уже характеристикой последней стадии рака кожи. Эта терминология применяется в описаниях историй болезни пациентов.
Сочетание T1a, к примеру, характеризует проявление меланомы на 1-й стадии, а вот сочетание T4b– является уже характеристикой последней стадии рака кожи. Эта терминология применяется в описаниях историй болезни пациентов.
N-категория
Данная категория призвана указать на наличие опухоли в лимфоузлах. Как известно, именно лимфоузлы в первую очередь подвержены поражению меланомой. Маркировка используется по результатам биопсии. Обозначение N0характеризует раннюю стадию меланомы. Идёт указание на то, что опухоль не задела близлежащие лимфатические узлы. Обозначение N3характеризует уже более поздние стадии развития рака кожи. Идёт указание на наличие в расположенных рядом лимфоузлах 2-3-х метастаз. Обозначение N2bговорит о патологическом увеличении лимфатических узлов. Это увеличение уже можно рассмотреть без микроскопа.
M-категория
Эта категория даёт указание на то, имеет ли меланома распространение на остальные органы. Кроме того, идёт указание, что это за органы и как изменился уровень фермента ЛДГ.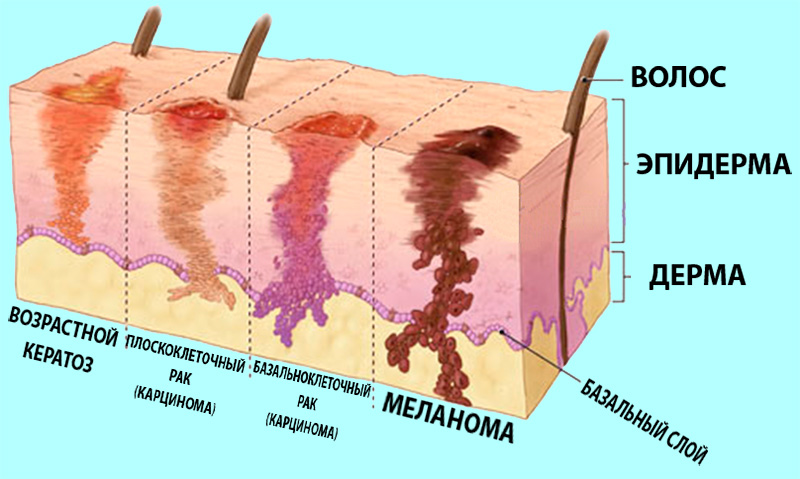 Это фермент лактатдегидрогеназа, участвующий в гликолизе. Метастазы на ранней стадии меланомы, обычно, не появляются.
Это фермент лактатдегидрогеназа, участвующий в гликолизе. Метастазы на ранней стадии меланомы, обычно, не появляются.
Стадии меланомы
| Стадии меланомы | Характеристика стадии |
|---|---|
| Меланома 0 | Наличествует только в верхнем слое кожи – эпидермисе (in situ). Данная меланома неинвазивна, она не проникает в глубокие слои кожи и не распространяется на другие части тела. |
| Меланома I | Выделяют здесь две подкатегории – A и B. Толщина опухоли на ранней стадии не превышает 1 мм. Новообразование не имеет шелушений и язв, не кровоточит. Скорость деления клеток достаточно низкая. Меланома не затрагивает органы и лимфатические узлы. На этой стадии рекомендуется операция, т.е., удаление злокачественного новообразования хирургическим путём. |
| Меланома II | Здесь выделяют три подкатегории – A, B и C. На этой стадии опухоль проникает вглубь. Толщина меланомы может достигать 2,00 мм, а иногда и 4,00 мм.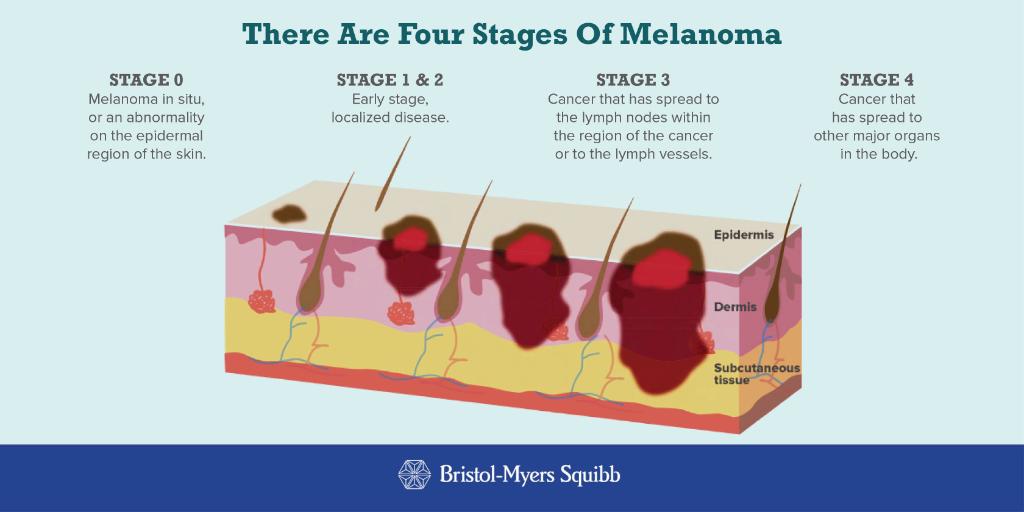 Сама поверхность меланомы приобретает гипертрофированный вид. Проявляется шелушение, наличие язв, порой, кровоточивость. Поражения лимфатических узлов и других органов не происходит. Сама поверхность меланомы приобретает гипертрофированный вид. Проявляется шелушение, наличие язв, порой, кровоточивость. Поражения лимфатических узлов и других органов не происходит. |
| Меланома III | Здесь также выделяют три подкатегории – A, B и C. На данной стадии опухоль поражает лимфатические узлы. Они могут быть увеличены, но не всегда. Злокачественное новообразование утолщается, проникает в ткани ещё глубже. Изъявления могут также либо проявляться, либо – нет. На этой стадии принято как лечение лучевой и операбельные (хирургические) методы. |
| Меланома IV | Данная стадия является последней стадией рака кожи. Злокачественное новообразование уже пускает метастазы, затрагивая внутренние органы, такие как: печень, лёгкие, головной мозг. Проникает на отдалённые лимфоузлы и поражает отдельные участки кожи. На этой стадии необходимо длительное и комплексное лечение. Возможно прибегнуть и к хирургическим методам, удалив отдельные поражённые опухолью кожные очаги или вырезав метастазы из внутренних органов. |
Лечение меланомы на разных стадиях
В зависимости от того, на какой стадии выявлена опухоль, производится соответствующее лечение. Терапия рекомендована на ранних стадиях меланомы, пока злокачественное новообразование ещё находится в самых верхних слоях эпидермиса, оно ещё не успело проникнуть вглубь и задеть внутренние органы и лимфатические узлы.
Хирургическое вмешательство, а также иммунная терапия показаны на второй и третьей стадии развития меланомы. На последней – 4-й стадииуже необходима комплексная терапия, так как меланома уже успевает задеть и внутренние органы, и костную систему. Здесь рекомендовано уже и хирургическое вмешательство, и лучевая терапия, и приём препаратов, препятствующих развитию опухоли. Меланому лечат по общепринятому протоколу, принятому всеми странами, где осуществляется лечение.
Меланому на 0-й стадии лечат иммуномодуляторами, а также операбельным путём.
На I-й стадии рекомендовано хирургическое удаление злокачественного новообразования, а также участков здоровой кожи, находящейся рядом с опухолью. Проводится также и биопсия сторожевого или, по-другому, сигнального лимфатического узла. Возможно также его полное удаление, при необходимости. Разумеется, нужна и поддержка препаратами.
Проводится также и биопсия сторожевого или, по-другому, сигнального лимфатического узла. Возможно также его полное удаление, при необходимости. Разумеется, нужна и поддержка препаратами.
На II-ой стадии меланомы показаны те же методы лечения, что и при I-й стадии: удаление опухоли хирургическим методом вместе со здоровым участком кожи, располагающемся рядом с новообразованием, биопсия сторожевого лимфоузла, а также его удаление по необходимости. Применение медикаментозных препаратов также необходимо, чтобы исключить рецидив.
На III-ей стадии, помимо удаления опухоли и участков здоровой кожи рядом с ней, сторожевого лимфатического узла, а по необходимости и участков, где найдены раковые клетки, показана химиотерапия, иммунотерапия и молекулярно-прицельная или таргетная терапия.
Для IV-ой стадии характерны следующие методы лечения: лучевая терапия, препараты-ингибиторы сигнальной трансдукции, иммунотерапия, таргетная терапия, а также паллиативное лечение.
В последующие три года после удаления злокачественного новообразования пациенту необходимо проходить обследование, чтобы исключить возможный рецидив возвращения меланомы.
Выживаемость пациентов, заболевших меланомой
Следует отметить, что раку кожи больше подвержены женщины, нежели мужчины. Каждый год диагностируется свыше 132 000случаев данного заболевания в мире. Данные предоставлены ВОЗ. Примерно 10%случаев заболевания – это наследственность, т.е., кто-то из близких был болен раком кожи. Показатели последних десяти лет, однако, дают определённую надежду, так как благодаря новым современным разработкам и более ранней диагностике выживаемость пациентов, подвергшихся данному онкологическому заболеванию, повысилась. В среднем до пяти лет. На самой ранней стадии более чем в 90% случаев прогноз на выздоровление – положительный.
Статистические данные по пятилетней выживаемости следующие:
- I стадия меланомы – до 92%;
- II стадия меланомы – 53-81%;
- III стадия меланомы – 40-78%;
- IV стадия меланомы – 15-20%;
Необходимо также отметить, что порой положительные прогнозы по IV-ой стадиирака кожи даже выше, чем по III-ейили даже II-ой стадии. Ведь иногда раковые клетки пускают метастазы в лимфатические узлы и отдалённые участки кожи, не затрагивая при этом самые важные системы и органы. Делая прогноз на положительный исход, также руководствуются и показателями уровня ЛДГ(фермент лактатдегидрогеназа). Если уровень ЛДГв норме, то шансы на выздоровление – гораздо выше.
Немаловажным фактором для положительного прогноза является также и возраст пациентов. К сожалению, у людей старшего поколения шансы несколько ниже, нежели у молодых. Стадия развития меланомы, кстати, в этом случае особой роли не играет. Меланоме больше подвержены люди со светлой кожей, однако, если меланоме подвергся смуглый человек, то его шансы на положительный исход несколько ниже, чем у его светлокожего собрата. Ухудшают прогнозы на выздоровление такие факторы как: серьёзные хронические заболевания, пересадка органов и заболевания ВИЧ.
Меланома и её признаки
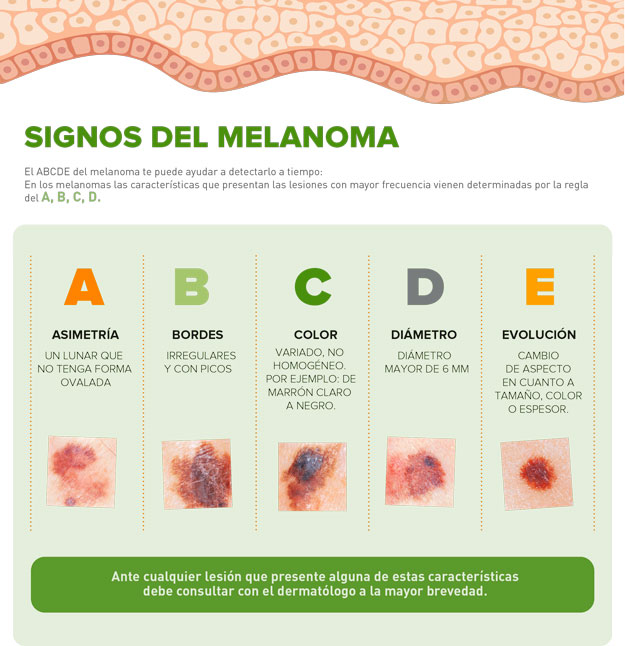
Это весьма опасное онкологическое заболевание, развивающееся крайне стремительно, но при этом совершенно незаметно. Меланома очень быстро пускает метастазы в лимфатические узлы, а затем поражает и внутренние органы и ткани. Положительно повлиять на выздоровление больного здесь может ранняя и своевременная диагностика. На начальной стадии меланома имеет ряд характерных симптомов. Основным маркером для определения стадии меланомы выступает правило – «ABCD».
Меланома очень быстро пускает метастазы в лимфатические узлы, а затем поражает и внутренние органы и ткани. Положительно повлиять на выздоровление больного здесь может ранняя и своевременная диагностика. На начальной стадии меланома имеет ряд характерных симптомов. Основным маркером для определения стадии меланомы выступает правило – «ABCD».
- Asymmetry – A – асимметрия. Края невуса (родинки) выглядят несимметрично.
- Border – B – граница. Края новообразования, как правило, с зазубринами, имеют нечёткий и неровный контур.
- Color – C – цвет. Родинка имеет неравномерный окрас, с оттенками серого и коричневого. Порой даже встречаются пятна красного, розового или белого цвета.
- Diameter – D – диаметр. Новообразование имеет размер в диаметре не менее 6 мм, и он постоянно увеличивается.
- Evolving – Е – развитие. Форма меняется с течением времени, доброкачественные родинка выглядит одинаково.
На начальной стадии рака кожи проявляются следующие симптомы: кровоточивость, появление язв и чешуек на поверхности новообразования, жжение, болезненность, зуд. К тому же, что является основным фактором определения зарождения опухоли, новообразование имеет ярко выраженный внешний вид на фоне других родинок (невусов). Заметив подобные признаки, незамедлительно обратитесь к врачу-онкологу. Ранняя диагностика – прекрасный шанс на выздоровление.
Источники:
http://www.cancerresearchuk.org/about-cancer/melanoma/stages-types
https://www.cancer.net/cancer-types/melanoma/stages
https://www.medicinenet.com/melanoma/article.html
https://www.medicalnewstoday.com/articles/154322.php
https://www.cancer.org/cancer/melanoma-skin-cancer/detection-diagnosis-staging/melanoma-skin-cancer-stages.html
МАТЕРИАЛЫ КОНГРЕССОВ И КОНФЕРЕНЦИЙ: V РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
V РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
ХИРУРГИЧЕСКАЯ «ПОГОНЯ» ЗА МЕТАСТАЗАМИ МЕЛАНОМЫ
Л.В. Демидов
Российский онкологический центр им.Н.Н.Блохина РАМН, Москва
Меланома кожи в стадии локального процесса (I-II клинико-патологические стадии) может быть излечена хирургически, если к моменту операции по удалению первичной опухоли она не инвазировала глубокие слои дермы, содержащие лимфатические и кровеносные сосуды и, следовательно, не имела благоприятных условий для метастазирования.
Ситуация с прогнозом болезни в корне меняется, если появляются метастазы. Как правило, на начальном этапе процесс метастазирования захватывает лимфатические узлы ближайшего регионарного коллектора. Это уже III клинико-патологическая стадия болезни, которая на этой стадии также подлежит хирургическому лечению в объеме лимфаденэктомии, однако вероятность стойкого излечения после операции не превышает 25%, потому что, как правило, уже имеются микрометастазы в отдаленных тканях и внутренних органах.
Клиническая манифестация этих метастазов обычно происходит в сроки от 6 до18 месяцев после выполненной лимфаденэктомии и знаменует собой IV диссеминированную стадию болезни. Отдаленные метастазы могут возникнуть в мягких тканях, коже и лимфатических узлах, а также внутренних органах. Здесь они чаще выявляются в легких, печени, головном мозге, но могут также поражать надпочечники и лимфатический аппарат тонкого кишечника, иногда кости. Главной особенностью отдаленных метастазов меланомы является их множественность.
Поэтому чаще всего больные с IV стадией болезни являются кандидатами для системного лекарственного лечения. Однако в силу изначальной невысокой чувствительности меланомы к существующим противоопухолевым препаратам, крайне редко удается достигать полной регрессии метастазов и добиваться стойкого длительного излечения. Данное обстоятельство невольно повышает интерес к альтернативным методам, в частности хирургическому, в лечении отдаленных метастазов меланомы.
В ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России этот подход далек от систематического применения. Иными словами существует крайне небольшое количество больных, у которых в лечении отдаленных метастазов меланомы предпочтение отдавалось хирургическому методу, а не химиотерапии.
Вместе с тем существует опыт других клиник, преимущественно крупных онкологических центров США, который позволяет составить мнение о том, насколько оправдана хирургическая «погоня» за отдаленными метастазами меланомы.:max_bytes(150000):strip_icc()/iStock_24463523_LARGE-5809a6205f9b58564cf5ff19.jpg)
Лечение больных диссеминированной меланомой кожи зависит от нескольких факторов. Это локализация метастазов, их количество, скорость роста, характер предшествующего лечения и его результат, а также общее состояние больного и желание лечиться. Количество вовлеченных в метастатический процесс органов является наиболее значимым фактором, определяющим прогноз жизни больного. Средняя продолжительность жизни больных с метастазами в один орган составляет 7 месяцев, в два — 4 месяца, а в три и более — всего лишь 2 месяца. Относительно благоприятный прогноз может наблюдаться в случае изолированных кожных и мягкотканных метастазов, а также метастазов в лимфатические узлы, промежуточный прогноз — при легочных метастазах, и однозначно неблагоприятный — при поражении печени и головного мозга. Полное удаление метастазов «благоприятной» локализации дает вполне обоснованную надежду на длительное выживание у небольшого процента больных, что само по себе не является казуистическим.
В таблице 1 суммирован опыт 5 онкологических клиник США по хирургическому лечению отдаленных метастазов меланомы. В общей сложности количество больных этих серий составило 377. Серии больных из M.D.Anderson и John Wayne онкологических центров были самыми крупными и практически одинаковыми по количеству: 116 и 118 больных соответственно. Для оценки эффективности хирургического лечения были выбраны наиболее типичные варианты отдаленного метастазирования меланомы (кожа, подкожная клетчатка, легкие, головной мозг и желудочно-кишечный тракт), и для каждого из них приведена средняя продолжительность жизни (в мес.), а также представлена 2-летняя выживаемость. Следует подчеркнуть, что, хотя метастазы меланомы в печень встречаются довольно часто, тем не менее, в настоящий анализ они не были включены из-за очевидной среди хирургов тенденции к отказу от оперативного лечения у данной категории больных. Серия больных из John Wayne института отличалась от больных M.D.Anderson центра в худшую сторону, т.
Таблица 1. Средняя продолжительность жизни (мес.) больных с отдаленными метастазами меланомы кожи после их полного удаления
| Локали- зация мета- стазов* |
M.D. Anderson Cancer Center 1 |
Memorial Sloan -Kettering Cancer Center Hospital 2 |
University оf Alabama Hospitals 3 |
Roswell Park Memorial Institute 4 |
John Wayne Cancer Institute 5 |
|---|---|---|---|---|---|
| Кожа, подкожная клетчатка |
23 (65) | 25 (12) | 17 (13) | 31 (25) | 24 (36) |
| Легкие | 16 (26) | 19 (17) | 9 (17) | 9 (13) | 19 (46) |
| Головной мозг | 15 (16) | 7,5 (5) | 8 (17) | 5 (4) | 12 (17) |
Жел. -киш. -киш.тракт(исключая печень) |
18 (9) | 15 (12) | 8 (5) | 8 (3) | 10 (19) |
| 2-летняя выжива- емость (%) |
15 | 21 | 16 | 31 | 45 |
*Количество больных указано в скобках
Несмотря на это выживаемость этой серии больных была существенно выше, и ее 2-летний показатель составил 45%. Безусловно, данный показатель превышает ожидаемый и объясняется тем, что в John Wayne клинике существует научная программа по циторедуктивным операциям при метастазах меланомы c последующей вакцинотерапией. Все остальные центры имели приблизительно одинаковый показатель 2-летней выживаемости, в среднем — около 20%, что приближается к известным статистическим показателям для меланомы кожи IV стадии.
Как относиться к такому результату? Оценивая известную для метастатической меланомы кожи эффективность лекарственной терапии, можно прогнозировать, что аналогичный показатель выживаемости после нее будет находиться в пределах от 10% до тех же 20%. Следовательно, хирургическая «погоня» за метастазами меланомы теоретически может принести пользу в виде улучшения показателя 2-летней выживаемости больных не больше, чем на 5-10%. Поэтому ее целесообразно осуществлять только в рамках научно-исследовательской программы.
Крайняя узость интервала между агрессивностью метастатической меланомы и лечебными возможностями против нее делает проблему применения хирургического метода лечения отдаленных метастазов в рутинном аспекте особенно деликатной.
Список литературы:
1. Feun LG, Gutterman J, Burgess MA, et al. The natural history of resectable metastatic melanoma (stage IV melanoma). Cancer 50:1656, 1976.
Cancer 50:1656, 1976.
2. Overett TK, Shiu MH. Surgical treatment of distant metastatic melanoma. Cancer 565:1222, 1985.
3. Wornom IL, Smith JW, Soong S-J, et al. Surgery as palliative treatment for distant metastases of melanoma. Ann Surg 204:181, 1986.
4. Wilson KS, Naidoo A. Hypertrophic osteoarthropathy. Mayo Clin Proc 54:208, 1979.
5. Wong JH, Skinner K, et al. The role of surgery in the treatment of nonregionally recurrent melanoma. Surgery 113:389, 1993.
Крупный успех в лечении меланомы на поздней стадии — выживает более половины пациентов
Автор фото, Getty Images
В лечении одной из самых страшных раковых опухолей — меланомы — достигнут большой успех.
Десять лет назад всего один из 20 пациентов, которому диагностировали меланому на поздней стадии, выживал в течение пяти лет.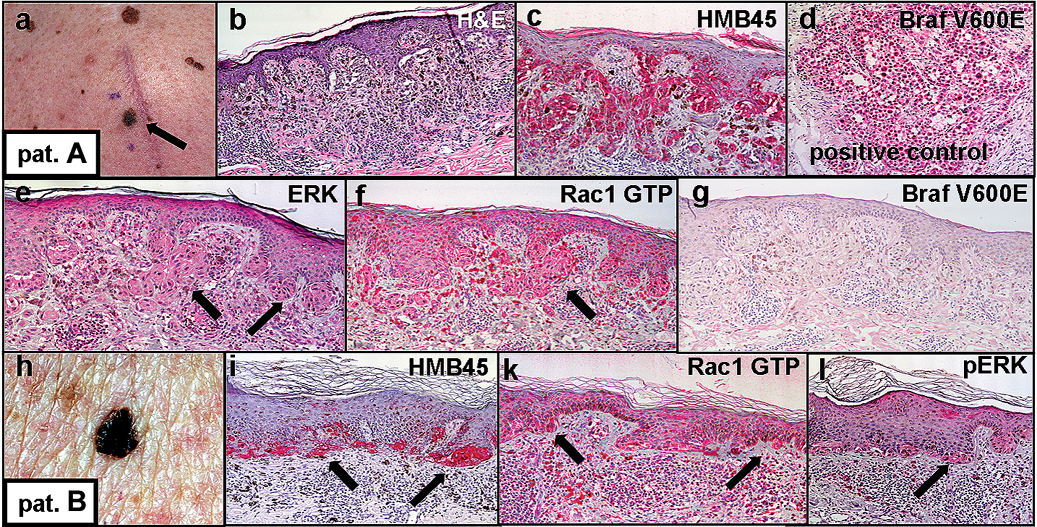 Большинство умирали в течение нескольких месяцев после постановки диагноза.
Большинство умирали в течение нескольких месяцев после постановки диагноза.
Теперь, по данным британских врачей, 52% пациентов с таким диагнозом имеют шанс прожить по крайней мере пять лет, благодаря иммунотерапии.
Насколько опасна меланома?
Меланома — пятый по распространенности вид рака в Британии. От неё гибнет около 2300 человек в год.
Если диагноз ставится на раннем этапе заболевания, шансы на выживание высоки. Однако если к моменту обнаружения рак начал агрессивно распространяться в организме пациента и образовывать метастазы, смерть наступала в течение в течение 6-9 месяцев после постановки диагноза.
«В прошлом метастазирующая меланома считалась неизлечимым заболеванием, — говорит профессор Джеймс Ларкин, консультант медицинского управления Ройял Марсден. — Онкологи считали меланому особым видом рака, который было невозможно лечить на стадии образования метастаз».
Что показали клинические испытания?
В клинических испытаниях, которые проходили в течение пяти лет в британских больницах, приняли участие 945 пациентов с меланомой четвертой стадии.
Треть из них получала ниволумаб, треть — ипилимумаб, а еще трети вводились оба лекарства.
Спустя пять лет врачи проанализировали выживаемость пациентов.
Оказалось, что выжили:
- 26% больных, получавших ипилимумаб
- 44% больных, получавших ниволумаб
- 52% больных, получавших и тот и другой препарат
«Мы были поражены столь быстрым прогрессом в течение такого короткого времени, — рассказывает профессор Ларкин. — Речь идет о самой необычной трансформации в лечении вида рака, который до этого считался самым трудно излечимым онкологическим заболеванием».
Результаты клинических испытания были доложены на заседании Европейского общества медицинской онкологии и опубликованы в журнале New England Journal of Medicine.
Свидетельства пациентов
Автор фото, Pam Smith
Подпись к фото,Пам Смит: я могла никогда не увидеть своих внуков
67 летняя Пам Смит, проходившая лечение в больнице города Танбридж-Уэллс, была включена в программу испытаний в январе 2014 года.
Она была в отчаянии, узнав, что ее рак является неизлечимым. У нее не было никаких шансов выжить, если бы не новые методы лечения, говорит Пам.
В течение четырех месяцев каждые две недели ей вводили препараты, но лекарства вызвали у нее такие сильные побочные эффекты в форме диареи, что лечение пришлось прекратить.
Однако ее опухоль сократилась вдвое и перестала расти. По словам Пам, она прекрасно себя чувствует.
«Я могла никогда не увидеть своих внуков, — говорит она. — Прошло уже больше пяти лет с момента диагноза, и моему внуку исполнилось шесть лет».
Можно ли считать результат полным излечением?
В случае рака всегда трудно говорить о полном излечении, но ремиссия в течение пяти лет является крупным достижением.
Некоторые из пациентов, которые принимают эти препараты, находятся в полной ремиссии и сканирование не выявляет у них патологий.
Другие, подобно Пам, имеют опухоли, но те не проявляют признаков роста.
Из всех выживших пациентов три четверти больше не нуждаются в приеме антираковых препаратов.
Иммунотерапия доказывает свою эффективность
Обычно наша иммунная система самостоятельно ищет в организме мутировавшие клетки и разрушает их, не давая им размножаться. Однако раковые клетки нашли способ обходить эту естественную защиту, что позволяет опухоли быстро расти.
Лауреаты Нобелевской премии по медицине 2018 года американец Джеймс Аллисон и японец Тасуку Хондзё научились обманывать раковые клетки и не давать им блокировать иммунную реакцию. Это произвело настоящую революцию в терапии и легло в основу нового класса лекарственных препаратов.
Пока что у этих лекарств немало побочных эффектов, однако они доказали свою эффективность в борьбе с онкологией. Иногда удается вылечить даже пациентов на поздней стадии рака, которых ранее считали неизлечимыми.
Как насчет побочных симптомов?
Да, новые препараты воздействуют на всю иммунную систему человека и могут вызывать такие побочные эффекты как усталость, воспаления кожи и диарею.
Иногда побочные эффекты оказываются настолько серьезными, что пациент, подобно Пам Смит, не может пройти полный курс лечения.
Однако даже кратковременное лечение, как оказалось, оказывает длительное благотворное воздействие на иммунную систему и на общее состояние больных.
Это сильно отличает иммунотерапию от других методов лечения, например, химиотерапии, которая перестает действовать при прекращении приема препаратов.
В то же время следует учитывать, что воздействие на иммунную систему может приводить к тому, что побочные эффекты могут проявляться и в дальнейшем.
Насколько доступны новые лекарства?
Результаты этого клинического испытания привели к тому, что новые иммунопрепараты начинают применяться по всему миру.
Государственная служба здравоохранения Британии необычно быстро одобрила применение новых препаратов. Теперь ими лечат и другие виды рака — легких и почек.
Через сколько лет меланома превращается в меланому с тяжелой стадией?
Меланома неоднородное заболевание. Есть поверхностная меланома в виде плоского пятна. Она может формироваться от 5 до 8 лет, а у пожилых и до 10 лет. И даже через 5-7 лет, когда пациент приходит и отмечает, что пятно у него долго менялось, и сейчас произошли значительные изменения, у таких пациентов мы можем получить первую или начальную вторую стадию, и после хирургического удаления могут быть хорошие параметры выздоровления. Например, 70-90 % людей полностью выздоравливает. А если пациент поздно обратился… Иногда и врачи не могут оценить, они могут игнорировать эти вещи. В нашем учреждении мы ежемесячно проводим курс повышения квалификации для районных терапевтов Москвы, мы рассказываем про 5 основных злокачественных опухолей, занимающих первые места по заболеваемости в мире и в Российской Федерации. Мы напоминаем о них, рассказываем, как распознать, что сделать, куда направить.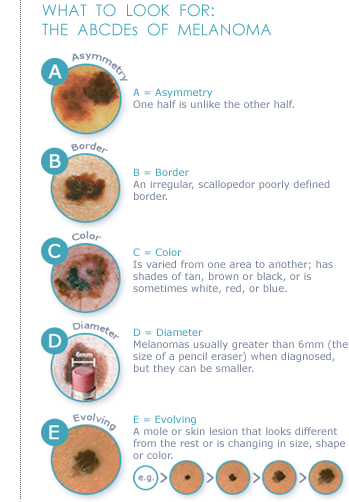 Мы повышаем онкологическую настороженность нашим терапевтам, ведь всё начинается с терапевта. Терапевт уже направляет к более узким специалистам. Хотелось, чтобы пациенты с меланомой быстрее преодолевали эти барьеры и попадали к нужному специалисту, не проходили долгие обследования.
Мы повышаем онкологическую настороженность нашим терапевтам, ведь всё начинается с терапевта. Терапевт уже направляет к более узким специалистам. Хотелось, чтобы пациенты с меланомой быстрее преодолевали эти барьеры и попадали к нужному специалисту, не проходили долгие обследования.
Если у человека уже тяжелая стадия меланомы, поражены другие органы, есть шансы на излечение. 10-15 лет назад шансов на излечение у больных четвертой стадией меланомы не было. Они жили 6-8 месяцев. Сейчас с развитием молекулярной биологии и иммунологии, мы знаем больше о меланоме, и к этой опухоли мы относимся очень персонализировано, индивидуально. Сейчас меланома – не единое однородное заболевание, это гетерогенная группа, где есть, как минимум, 5 болезней с различными вариантами развития. Мы смотрим, где меланома располагалась, изучаем её молекулярно-генетический портрет, её мутации. Практически на каждую мутацию есть новые препараты, которые могут её заблокировать. Терапия называется таргетной или молекулонацеленной, мишень-терапией. Существует понимание, как функционирует иммунная система при злокачественных опухолях. Мы знаем, что её сдерживает или подавляет, появились препараты, уже зарегистрированные в Российской Федерации, которые могут снимать тормозы с иммунной системы, заставляют её быть более активной, направлять её к опухоли. И пациенты, которые получают современное лечение, могут жить годами. Барьер в 8 месяцев сейчас преодолевается для многих пациентов. Меланому на 4-й стадии мы можем превращать в длительную хроническую многолетнюю болезнь, можем сделать так, что метастазы могут законсервироваться, стабилизироваться и годами не расти. Такой пациент регулярно приходит к онкологу, наблюдается, сдает анализы и проходит обследования. Но мы можем эту метастатическую меланому превратить в хроническую форму болезни, у нас много хронических заболеваний: ишемическая болезнь сердца, бронхиальная астма, сахарный диабет. Они тоже фатальные и приводят к смерти населения, но с развитием науки мы можем на них действовать, пациент может жить десятки лет.
Существует понимание, как функционирует иммунная система при злокачественных опухолях. Мы знаем, что её сдерживает или подавляет, появились препараты, уже зарегистрированные в Российской Федерации, которые могут снимать тормозы с иммунной системы, заставляют её быть более активной, направлять её к опухоли. И пациенты, которые получают современное лечение, могут жить годами. Барьер в 8 месяцев сейчас преодолевается для многих пациентов. Меланому на 4-й стадии мы можем превращать в длительную хроническую многолетнюю болезнь, можем сделать так, что метастазы могут законсервироваться, стабилизироваться и годами не расти. Такой пациент регулярно приходит к онкологу, наблюдается, сдает анализы и проходит обследования. Но мы можем эту метастатическую меланому превратить в хроническую форму болезни, у нас много хронических заболеваний: ишемическая болезнь сердца, бронхиальная астма, сахарный диабет. Они тоже фатальные и приводят к смерти населения, но с развитием науки мы можем на них действовать, пациент может жить десятки лет. Так же и с меланомой, в определенных ситуациях мы можем вызывать значительное торможение.
Так же и с меланомой, в определенных ситуациях мы можем вызывать значительное торможение.
Главное, чтобы пациент пришел к онкологу за помощью, а не к знахарю, целителю, травнику. Это полное шарлатанство, аферизм, это определенный бизнес, нечистый на руку. Эти методики не работают, они позволяют сбить пациента с толку, а он теряет драгоценное время.
ВЫЖИВАЕМОСТЬ ПАЦИЕНТОВ ПОСЛЕ УДАЛЕНИЯ ГЛАЗНОГО ЯБЛОКА ПО ПОВОДУ УВЕАЛЬНОЙ МЕЛАНОМЫ В ПЕРМСКОМ КРАЕ | Гаврилова
1. Lutz J.M., Gree I.M., Foss A.J. Risk factors for intraocular melanoma and occupational exposure. Br. J. Ophthalmol. 1999;83(10):1190‑1193.
2. Brovkina A. F., Vаl’skij V. V., Gusev G. A. [Guide for physicians. Ophthalmooncology] M.: Medicina, 2002. (in Russ. ).
).
3. Brovkina A.F., Astahov Ju.S. [Manual of clinical ophthalmology]. M.: Medical information agency, 2014. (in Russ.).
4. Brovkina A.F. [Choroidal melanomas: problems, controversial questions] Sovremennye aspekty lechenija melanom horioidei: problemy i diskussionnye voprosy [Annals of ophthalmology]. Vestnik oftal’mologii. 2006;1:13‑15. (in Russ.).
5. Saakjan S.V., Panteleeva O.G., Shirina T.V. [Metastatic disease characteristics and survival in patients with uveal melanoma depending on primary tumor treatment]. Osobennosti metastaticheskogo porazhenija i vyzhivaemosti bol’nyh s uveal’noj melanomoj v zavisimosti ot provedennogo lechenija [Russian ophthalmological journal]. Rossijskij oftal’mologicheskij zhurnal. 2012;5(2):55‑7 (in Russ.).
6. Merabishvili V., Merabishvili E. [Survival of patients with malignant tumors of the eye taking into account gender, age and histological structure of neoplasms]. Vyzhivaemost’ bol’nyh zlokachestvennymi novoobrazovanijami glaza s uchetom pola, vozrasta i gistologicheskoj struktury opukhole.j [Ophthalmology]. Oftal’mologija in Russia. 2016;13(1):38‑43. (In Russ.). DOI: http://dx.doi.org/10.18008/1816‑5095‑2016‑1
Merabishvili V., Merabishvili E. [Survival of patients with malignant tumors of the eye taking into account gender, age and histological structure of neoplasms]. Vyzhivaemost’ bol’nyh zlokachestvennymi novoobrazovanijami glaza s uchetom pola, vozrasta i gistologicheskoj struktury opukhole.j [Ophthalmology]. Oftal’mologija in Russia. 2016;13(1):38‑43. (In Russ.). DOI: http://dx.doi.org/10.18008/1816‑5095‑2016‑1
7. Stojuhina A.S., Chesalin I.P. [Survival rates for large choroidal melanomas]. Vyzhivaemost’ bol’nyh bol’shimi melanomami horioidei [Annals of ophthalmology]. Vestnik oftal’mologii. 2014;4:39‑44. (in Russ.). doi: 10.17116/oftalma2015131190‑94
8. Kujala E., Makite T., Kivela T. Very long‑term prognosis of patients with malignant uveal melanoma. Invest. Ophthalmol. Vis.Sci. 2003:44:4651‑4659.
9. Assessment of metastatic disease status at death in 435 patients with large choroidal melanoma in the Collaborative Ocular Melanoma Study (COMS): COMS report. 15. Arch Ophthalmol. 2001;119;670‑6.
10. Gragoudas E.S., Egan K.M., Seddon J.M., et al. Survival of patients with metastases from uveal melanoma. Ophthalmology. 1991;98:383‑9.
11. Amirjan A.G., Saakjan S.V. [Prognostic factors for uveal melanoma]. Faktory prognoza uveal’noj melanomy. [Annals of ophthalmology]. Vestnik oftal’mologii. 2015;1:90‑94. (in Russ.). doi: 10.17116/oftalma2015131190‑94
12. Shhepetneva M.A., Kovalevskaja M.A., Efimova H.A. [Analysis of the incidence of melanoma of the choroid in the Voronezh Region]. Analiz zabolevaemosti melanomoj sosudistoj obolochki v Voronezhskoj oblasti. Sistemnyj analiz i upravlenie v biomedicinskih sistemah: zhurnal prakticheskoj i teoreticheskoj biologii i mediciny. [System analysis and management in biomedical systems: Journal of Practical and Theoretical Biology and Medicine]. 2008;7(3):640‑642. (in Russ.).
13. Furdova A., Slezak P., Chorvath M., Waczulikova I., Sramka M., Kralik G. No differences in outcome between radical surgical treatment (enucleation) and stereotactic radiosurgery in patients with posterior uveal melanoma. Neoplasma. 2010;57(4):377—381. doi:10.4149/neo_2010_04_377
Симптомы рака кожи и методы его диагностики
Страшное слово «рак» знакомо даже людям, далеким от медицины. Принято считать, что этот термин — синоним скорой неотвратимой смерти, ведь на слуху у всех трагические истории из жизни знаменитостей или знакомых, которым был поставлен такой диагноз.Различные злокачественные новообразования кожи были диагностированы у Хью Джекмана (Люди Икс, Росомаха), Хлои Кардашьян (американская телевизионная персона, участница реалити-шоу «Семейство Кардашян), всем известный отец «Ералаша» продолжает борьбу за жизнь с метастазами меланомы – «Получилось, что из маленькой родинки выросла большая болезнь» – вздыхает Грачевский. От последствий развития опухоли кожи погибли: Боб Марли (ямайский музыкант, гитарист), победительница конкурса «Мисс Вселенная 2006» –российская модель Анна Литвинова. В 2012 году у Анны была диагностирована меланома, она уехала на лечениев Германию где умерла около года спустя, 22 января 2013 года, в 31-летнем возрасте.
Однако, рак можно победить, если выявить его на ранней стадии и обратиться за квалифицированной медицинской помощью. Потому поговорим об одном из самых распространенных онкологических заболеваний в России — злокачественных новообразованиях кожи, которыезанимают второе место по распространенности среди всех злокачественных новообразований у женщин (после рака молочной железы) и третье – у мужчин (после рака легких и рака предстательной железы).
Ситуация в России остается тревожной: зачастую пациенты попросту игнорируют первые симптомы рака кожи и обращаются в больницу с запущенной стадией опухоли, когда гарантии выздоровления быть не может. Так при 4-ой стадии меланомы – наиболее злокачественного новообразования кожи, даже при условии правильного лечения, лишь половина из 10-ти пациентов живет дольше 5-ти лет. А ведь в отличие от рака внутренних органов, злокачественные опухоли кожи всегда на виду.
Причины рака кожи
Появление любого злокачественного новообразования — следствие сбоя в работе организма: в норме иммунная система уничтожает дефектные клетки до того, как они приступают к бесконтрольному делению. Если же по каким-то причинам защитные механизмы не срабатывают, опухоль увеличивается в размерах и становится неуязвимой для собственной защитной системы. В случае с раком кожи наиболее опасными факторами внешней среды, повышающим вероятность развития опухоли, являются ультрафиолетовое и ионизирующее облучение, а также воздействие агрессивных химических веществ.
Эксперты отмечают, что злокачественные новообразованиякожи, в частности меланома нередко провоцируются посещением солярия: мода на бронзовый загар привела к значительному увеличению частоты появления злокачественных новообразований (в США именно по этой причине ежегодно выявляется более 170 тысяч заболевших). «…Белокожая Аня всегда старалась следовать моде, она, как и многие сейчас, посещала солярии, любила ездить в экзотические страны, где много солнца» — вспоминает подруга Анны Литвиновой, Ксения Волкова.
Симптомы и признаки рака кожи
Любая разновидность злокачественных опухолей вначале проявляется локально — в месте поражения, а затем, при отсутствии лечения, сказывается на самочувствии больного в целом. В случае с раком кожи соотношение между местными и общими симптомами — в пользу местных: до поздних стадий заболевания окружающие могут не подозревать, что человек болен. Местные симптомы рака кожи заметны невооруженным глазом: это может быть ранка, которая не заживает на протяжении нескольких недель или месяцев, пятно, постепенно увеличивающееся в размерах, или родинка, которая изменила форму или цвет. В зависимости от вида опухоли рост новообразования бывает медленным или быстрым, но в любом случае изменение кожных покровов прогрессирует. В пораженной области часто наблюдается зуд, боль, кровотечение или шелушение, подобные жалобы должны насторожить не только больного, но и его родных — откладывать визит к врачу в таких случаях категорически не рекомендуется.
Виды, стадии и прогноз
Злокачественные новообразования кожи включают сразу несколько онкологических заболеваний, имеющих разное происхождение, специфичные симптомы и прогноз. Такие опухоли, как базалиома, плоскоклеточный рак кожи и меланома диагностируются статистически чаще прочих, но встречаются и более редкие варианты. Достоверно установить диагноз способен только онколог-дерматолог.
Базалиома (базальноклеточный рак кожи) — самый распространенный вид рака кожи, который развивается из клеток эпидермиса. Вначале, опухоль выглядит как небольшой розовый узелок, под поверхностью которого видна сеть кровеносных сосудов. По мере роста,новообразование может изъязвляться и кровоточить, на поверхности появляется без видимых причин корка, которая может проходить, но затем появляется вновь. Чаще базалиома возникает на коже лица, реже — на других участках кожи. Обычно болезнь развивается медленно и не дает метастазов, поэтому прогноз для больных — благоприятный, а лечение включает только удаление опухоли.
Плоскоклеточный рак кожи может иметь несколько клинических вариантов, в одном случае он может быть представлен, также, как и базалиома – одиночным узлом с кровоточащей язвочкой или коркой на поверхности, длительно-незаживающей язвой или локальным кератозом, напоминающий «кожный рог». Плоскоклеточный рак нередко располагается на красной кайме губ, открытых участках кожи, подверженных воздействию ультрафиолета. Этот рак способен к инвазивному росту и метастазированию – т.е. проникает в глубокие слои кожи и с током крови переноситься по телу к другим органам и тканям.
Меланома — опухоль, которая развивается из пигментированных клеток кожи – меланоцитов. Как правило, развивается на месте родинок, представляющих собой скопление пигмента или, появляется самостоятельно.
При прогрессировании меланома склонна к быстрому агрессивному росту и способна образовывать метастазы (отдаленные опухоли). Однако, до начала инвазивного роста обычно проходит несколько лет, пока меланома растет в пределах эпидермиса (самого верхнего слоя кожи) – «стадия горизонтального роста» и лечение, которое заключается в удалении опухоли, в этот момент практически полностью исключает риск формирования отдаленных метастазов и развитие грозных осложнений для жизни. Именно поэтому так важно следить за внешним видом родинок: если одна из них изменила форму, цвет или выглядит припухшей, стала чесаться или кровоточить, необходимо срочно обратиться к врачу.
Напротив, в старшей возрастной группе чаще формируется нодулярная или узловая меланома, которая практически не имеет стадии внутриэпидермального роста и быстро становиться инвазивной, поэтому очень важно также следить за появлением новых темных узловых новообразований на коже наших пожилых близких и родственников.
Людей, у которых диагностирован рак, всегда интересует прогноз течения заболевания. «Доктор, сколько я проживу?» — популярный вопрос в практике онкологов. Если речь идет о раке кожи, то перспективы выздоровления в большинстве случаев хорошие, потому как самая распространенная опухоль — базалиома —не дает метастазов, и для ее устранения достаточно небольшого хирургического вмешательства. Ключевым параметром в онкологии является показатель выживаемости. Он говорит о том, например, какое число больных с данной стадией рака смогло прожить более 5-ти лет после выявления опухоли. Так, при базалиоме показатель выживаемости приближается к 100% вне зависимости от размеров новообразования. А при меланоме 2 стадии через 5-летний рубеж даже при условии грамотного лечения перешагивает только 50% пациентов.
Методы диагностики
Врачи, специализирующиеся на диагностике рака кожи, имеют впечатляющий арсенал диагностических методик, позволяющих подтвердить или опровергнуть диагноз, а также классифицировать опухоль. Осмотр — самый очевидный и простой способ заподозрить наличие новообразования. Если вы волнуетесь, что у вас развивается рак кожи, — покажите необычный участок тела доктору. Он сравнит подозрительную родинку или язвочку с другими скоплениями пигментных клеток. Если будут основания для беспокойства, врач назначит дополнительные методы диагностики. Для более точной диагностики онкологи-дерматологи используют дерматоскоп — прибор, позволяющий разглядеть структуру новообразования детально, в поляризованном свете. Для окончательного подтверждения природы опухоли используется биопсия, при которой врач забирает небольшой участок ткани пациента из пораженной области, чтобы в условиях лаборатории изучить его под микроскопом. Ультразвук и томография необходимы, чтобы выявить возможные метастазы
Врачи иногда говорят, что при выявлении рака важно не дать диагнозу «парализовать сознание». Информированность о современных диагностических и лечебных возможностях и сотрудничество с врачами помогут победить коварную болезнь!
Как часто нужно показываться врачу, чтобы своевременно выявить заболевание?
Периодичность осмотров составляет 6-12 месяцев.
Как пройти осмотр в Центре им. В.П. Аваева?
В нашем Центре приём пациентов ведёт онколог-дерматолог, кандидат медицинских наук Дубенский Владислав Валерьевич
Запись по телефону: (4822) 633-123.
записаться на прием к онкологу-дерматологу
Понимание стадий и степени меланомы
Хотя меланома является относительно редкой формой рака кожи, ожидается, что в 2021 году будет диагностировано около 106 110 новых случаев, по оценкам Американского онкологического общества. Около 1 процента случаев рака кожи — это меланомы, большинство других — это базально-клеточный и плоскоклеточный рак кожи, но на меланомы приходится большая часть смертей от рака кожи.
Прежде чем рекомендовать лечение, врачам сначала нужно больше узнать о меланоме и о том, что происходит внутри кожи.
TNM постановка
Определение стадии меланомы может быть сложным. Этапы назначаются в зависимости от размера или толщины опухоли, распространилась ли она на лимфатические узлы или другие органы, а также некоторых других характеристик, таких как скорость роста.
Стадии варьируются от I до IV, более высокие числа указывают на более развитую меланому. За некоторыми номерами стадий следуют заглавные буквы от A до D для дальнейшего описания опухоли и ее потенциального распространения.
Американский объединенный комитет по раку разработал единую систему стадирования, которая позволяет врачам определять, насколько развита меланома, и делиться этой информацией друг с другом значимым образом.
Эта система определения стадии меланомы, известная как стадия TNM, измеряет три характеристики рака.
T (опухоль): Описывает толщину опухоли или то, насколько глубоко она вросла в кожу. Толщина меланомы, также известная как измерение Бреслоу, является важным фактором при прогнозировании распространения опухоли.Чем толще меланома, тем больше вероятность ее распространения. Скорость деления опухолевых клеток (также известная как скорость митоза) и наличие или отсутствие язвы (открытой кровоточащей язвы) также учитываются при определении категории T.
N (узел): Указывает, распространилась ли меланома на близлежащие лимфатические узлы или каналы, соединяющие лимфатические узлы.
M (метастаз): Относится к тому, распространилась ли меланома на отдаленные органы, а также к уровню лактатдегидрогеназы (ЛДГ), вещества в крови.Другими словами, если он дал метастазы.
У категорий TNM также есть подтипы.
Толщина опухоли (T)
- TX: невозможно измерить основную опухоль
- T0: Основная опухоль не обнаружена
- Tis: Меланома in situ (аномальные клетки, обнаруженные во внешнем слое кожи или эпидермисе)
- T1: ≤1,0 мм
- T2:> 1,0–2,0 мм
- T3:> 2,0-4,0 мм
- T4:> 4.0 мм
Поражение лимфатических узлов (N): Чем выше число после N, тем больше лимфатических узлов содержат рак.
- NX: рак в соседних лимфатических узлах невозможно измерить
- N0: В соседних лимфатических узлах нет рака
- N1-N3: Относится к количеству лимфатических узлов, содержащих рак.
Метастазы (M): Меланома может распространяться практически везде, но имеет тенденцию распространяться в легкие, печень, мозг, кости и кожу или лимфатические узлы в других частях тела.Буква M указывает на возможное распространение меланомы по всему телу.
- MX: распространение невозможно измерить
- M0: Рак не распространился на другие части тела
- M1: Рак распространился на другие части тела
Стадии меланомы
После того, как врачи соберут всю возможную информацию о раке, они назначат стадию. Этап дает врачу и пациенту общий язык, чтобы понять, насколько далеко рак, где он находится и какие варианты лечения доступны.
- Стадия 0: Это также называется меланомой in situ. Это означает, что есть клетки меланоцитов, которые могут стать злокачественными на вашей коже. Это самая ранняя стадия — здесь лучше всего ловить и лечить меланоциты, прежде чем они станут злокачественными.
- Стадия I. Как правило, меланома I стадии глубоко прорастает в кожу, но не распространилась на лимфатические узлы или другие части тела.
- При стадии IA толщина рака не превышает 1 мм, с изъязвлением или без него.
- При стадии IB толщина опухоли более 1 мм, но не более 2 мм, без изъязвлений.
- Стадия II: меланома стадии II глубже проникла в кожу и имеет более опасные черты, но еще не распространилась.
- При стадии IIA опухоль либо более 1 мм, но не более 2 мм толщиной, с изъязвлением, либо более 2 мм, но не более 4 мм толщиной, без изъязвления.
- На стадии IIB опухоль составляет более 2 мм, но не более 4 мм толщиной, с изъязвлением, или более 4 мм толщиной без изъязвления.
- На стадии IIC опухоль толщиной более 4 мм с изъязвлением. Меланома толщиной более 4 мм имеет высокий риск распространения.
- Стадия III: Диагноз меланомы стадии III означает, что раковые клетки распространились на близлежащие лимфатические узлы, но не на отдаленные органы или любую другую часть тела.
- Этап III делится на IIIA, IIIB, IIIC и IIID. Эти буквы отражают степень и степень роста лимфатических узлов.
- Стадия IV: На стадии IV меланома распространилась на другие органы и / или отдаленные лимфатические узлы.
- Хотя все это относится к стадии рака IV, M системы TNM может указывать, где рак распространился конкретно, например, на другие участки кожи (M1A), легкие (M1B), другие органы или области тело (M1C) или — в наиболее развитой форме — центральная нервная система (M1D).
Клиническая стадия и патологическая стадия
Чтобы усложнить определение стадии, рак также может иметь клиническую и патологическую стадии.
Клиническая стадия проводится перед операцией на основе анализов крови, физических осмотров или визуализационных тестов, таких как рентген, компьютерная томография (КТ), магнитно-резонансная томография (МРТ) или позитронно-эмиссионная томография (ПЭТ).
То, что врачи обнаруживают во время операции, может предоставить более подробную информацию о размере и распространении рака. Часто после операции будут исследованы некоторые ткани, оставшиеся после операции, чтобы получить больше подсказок. Этот процесс известен как патологическая стадия или хирургическая стадия.
Если операция невозможна, врачи будут использовать клиническую стадию при составлении плана лечения.
Рецидивирующий рак меланомы
Рецидив меланомы в пределах 2 см от исходного участка опухоли считается местным рецидивом. Рецидив лимфатического узла и отдаленный рецидив — это термины, используемые для описания рака, который имеет те же характеристики ДНК, что и исходная опухоль, но развивается в другом месте тела, например, в лимфатических узлах.
Рецидив лимфатического узла развивается в лимфатическом узле (ах) в области, ближайшей к исходной опухоли меланомы. Считается отдаленным рецидивом, когда клетки меланомы попадают в кровоток и развиваются в опухоли в другом месте тела. Попадая в систему кровообращения, раковые клетки меланомы могут перемещаться в отдаленные места. Они могут развиваться в любой ткани, но обычно они растут в легких, печени или головном мозге. Метастазы также могут возникать в кости, сердце, поджелудочную железу, почки или щитовидную железу, а также в других местах.
Подногтевая меланома — StatPearls — Книжная полка NCBI
Непрерывное обучение
Подногтевая меланома — это отдельный подтип кожной злокачественной меланомы, возникающей из структур внутри ногтевого аппарата. Слово subungual происходит от латинского «sub», означающего внизу, и «unguis», что означает гвоздь или коготь. Обычно это вариант акральной лентигинозной меланомы, злокачественной меланомы, возникающей на ладонях и подошвах. Это мероприятие направлено на получение актуального и точного обзора подногтевой меланомы и ее межпрофессионального управления командой.
Цели:
Определить этиологию подногтевой меланомы.
Просмотрите презентацию подногтевой меланомы.
Опишите доступные варианты лечения подногтевой меланомы.
Обобщите важность улучшения координации помощи между членами межпрофессиональной группы для улучшения результатов для пациентов, страдающих подногтевой меланомой.
Введение
Подногтевая меланома представляет собой отдельный подтип кожной злокачественной меланомы, возникающей из структур внутри ногтевого аппарата. Слово subungual происходит от латинского «sub», означающего внизу, и «unguis», что означает гвоздь или коготь. Обычно это вариант акральной лентигинозной меланомы, злокачественной меланомы, возникающей на ладонях и подошвах. Первоначально Бойер узнал его в 1834 году. Хатчинсон продолжил более подробно описывать признаки в 1886 году, предлагая более точное представление о состоянии.Он описал очень специфический признак, тесно связанный с подногтевой меланомой, когда пигмент выходит за пределы ногтя и проникает в прилегающую кожу («признак Хатчинсона»). Эта статья представляет собой современный и точный обзор подногтевой меланомы и методов ее лечения. [1] [2] [3]
Этиология
Злокачественная меланома матрикса ногтя, как и меланома кожи, возникает из меланоцитов. В отличие от кожной злокачественной меланомы, подногтевая меланома не связана с пребыванием на солнце.[4]
Эпидемиология
Подногтевые меланомы встречаются редко и составляют от 0,7% до 3,5% всех злокачественных меланом во всем мире. Меланома ногтевого аппарата встречается одинаково у всех расовых групп. Однако это наиболее распространенный вариант злокачественной меланомы у афроамериканцев, азиатов и выходцев из Латинской Америки. На его долю приходится 75% меланом в африканских популяциях, 25% в китайских и 10% в японских популяциях. Эти группы обычно имеют очень низкую заболеваемость кожной злокачественной меланомой из-за пигмента меланина, защищающего их кожу от ультрафиолетового (УФ) излучения солнца.Это наиболее часто встречается в седьмом десятилетии жизни у мужчин и в шестом десятилетии жизни у женщин. Чаще всего поражаются большой палец стопы и большой палец. Эти цифры составляют от 75% до 90% случаев. [5] [6]
Патофизиология
Подногтевая меланома возникает из-за повышенной выработки меланина меланоцитами. При активации меланоциты дифференцируются в матричные клетки и мигрируют дистально.
Гистопатология
Гистопатологический процесс подногтевой меланомы уникален из-за поражения ногтевого узла.Патология демонстрирует повышенное количество меланоцитов в базальном слое препарата. Этот слой содержит плеоморфные меланоциты с ядрами неправильной формы. При инвазивной меланоме ногтей будет наблюдаться высокое количество меланоцитов, в два-три раза больше, чем при доброкачественной меланонихии. Другие особенности включают многоядерность, атипию и обширное пагетоидное распространение меланоцитов. Воспаление также присутствует при запущенной меланоме, но не проявляется при доброкачественной меланонихии.
Гистология, скорее всего, соответствует акральной лентигинозной меланоме (67% случаев), подтипу меланомы, поражающей ладони и подошвы.В пятидесяти процентах случаев наблюдается поверхностное распространение, а в некоторых случаях наблюдается и то, и другое. Акральная лентигинозная меланома характеризуется акантозом, удлинением ребер и разрастанием атипичных меланоцитов в эпидермисе. Базальные кератиноциты заменяются злокачественными меланоцитами.
История и физика
Подногтевая меланома проявляется в коричнево-черном цвете ногтевого ложа. Он может проявляться как полосой пигментации, так и неправильной пигментацией.Изменение цвета может прогрессировать до утолщения, расщепления или разрушения ногтя с болью и воспалением.
Необходимо учитывать другие возможные причины пигментации ногтевого блока. Анамнез должен включать эпизоды травмы, чтобы учесть подногтевую гематому, а также инфекцию, чтобы учесть пигментные грибковые состояния ногтей.
Levit et al. описали рекомендации ABCDEF, которые можно использовать для оценки риска того, что пигментное поражение ногтей может стать меланомой. Вот эти рекомендации:
A: Возраст: от 50 до 70 лет и происхождение из Африки, Японии, Китая и коренных американцев
B: Коричнево-черная полоса более 3 мм с неровной окантовкой
C : Изменение размера и скорости роста
D: Цифра: большой палец, большой палец ноги или указательный палец
E: Распространение изменения цвета на кожу вокруг ногтя (знак Хатчинсона)
F: Семья гистология меланомы
Оценка
Основной способ поставить диагноз — провести биопсию на всю толщину ногтевого ложа.Недавнее исследование Reilly et al., Опубликованное в декабре 2017 года, продемонстрировало, что может быть большое несоответствие между толщиной опухоли при начальной биопсии и окончательной толщиной опухоли. Этот момент подчеркивает важность качественной биопсии для проведения первичной гистологической оценки с последующим планом лечения.
Биопсию ногтевого ложа следует выполнять с помощью блокады пальцевого нерва. Жгут полезен для гемостаза, но палец не следует обескровливать при злокачественных новообразованиях.Ногтевую пластину следует осторожно удалить с помощью надкостничного подъемника. Для визуализации зародышевого матрикса можно сделать два радиальных разреза под углом 45 градусов с каждой стороны от эпонихиальной складки. Затем следует взять полную биопсию пигментированной области. В идеале, по возможности, это должна быть эксцизионная биопсия. Затем дефект устраняется рассасывающимся швом и ноготь заменяется в эпонихиальной складке.
После эксцизионной биопсии пигментного поражения ногтевого ложа на основании гистологического отчета может быть составлен дальнейший план лечения.В отчете будут подробно описаны подтип злокачественной меланомы, толщина Бреслоу и другие гистологические характеристики. [7] [8]
Лечение / ведение
Междисциплинарная команда специалистов по меланоме будет использовать эту информацию, чтобы определить, какие дальнейшие исследования необходимы и какое лечение подходит. Основным методом лечения любого вида меланомы является иссечение. Первоначальное удаление — это биопсия, которая предлагает гистологический отчет, а рекомендации определяют широкий локальный край иссечения в соответствии с глубиной опухоли.То же самое и с подногтевой меланомой. [3] [9] [10]
Бассейны лимфатических узлов должны быть клинически оценены, а те, у кого есть клинически пальпируемые узлы, должны быть дополнительно оценены с помощью визуализации и с биопсией или без нее, а также проведена лимфодиссекция, если заболевание обнаружено. Согласно руководящим принципам, при поражениях толщиной от 1 до 4 мм без лимфаденопатии следует предлагать биопсию сторожевых лимфатических узлов.
Пациенты с толщиной опухоли более 4 мм должны рассматриваться для предоперационного определения стадии с помощью КТ-ПЭТ и МРТ головного мозга.
Управление обсуждается далее в следующих разделах.
Дифференциальный диагноз
Двумя наиболее распространенными ошибочными диагнозами подногтевой меланомы являются полосатая меланонихия и онихомикоз. Полосатая меланонихия — это отложение меланина в ногтевой пластине, которое обычно не представляет собой одиночную пигментированную полосу. Онихомикоз — это грибковая инфекция ногтей, вызывающая безболезненное дистрофическое изменение пигмента ногтя. Другие дифференциальные диагнозы включают подногтевую гематому, которая обычно представляет собой болезненное поражение, которое проявляется после травмы и мигрирует дистально по мере роста ногтя, и узловой невус, который представляет собой единичное доброкачественное поражение без полос.
Хирургическая онкология
Хирургическое лечение подногтевой меланомы было спорным в последнее десятилетие. В течение многих лет единственным приемлемым вариантом лечения была цифровая ампутация. В 1965 г. Дас Гупта и др. провели исследование, посвященное лечению подногтевой меланомы. В исследование были включены 34 пациента, которым ампутация межфалангового сустава производилась по сравнению с более проксимальной ампутацией. В этом исследовании сообщается, что все пациенты, перенесшие ампутацию межфалангового сустава, не выжили в течение 5 лет.После этого хирурги пришли к мнению, что эти редкие случаи рака должны подвергаться агрессивному лечению в виде проксимальных ампутаций на уровне запястно-пястного сустава или предплюсне-метатарзального сустава. Этот уровень ампутации может препятствовать функционированию пораженной руки или ноги, особенно потому, что чаще всего поражаются пальцы большого пальца и большого пальца стопы. Результаты этого исследования значительны; тем не менее, авторы не сообщили о глубине поражения, и половина пациентов имела метастатическое или рецидивирующее заболевание на момент обращения.Поэтому рекомендации по лечению, возможно, немного искажены. [11] [12] [13]
В последнее время эта агрессивная форма лечения стала менее приемлемой, что привело к исследованию менее радикальных хирургических вариантов для сохранения длины и получения хирургического разрешения. Cochran et al. опубликовали обзор литературы в 2014 году, в котором конкретно рассматривались варианты лечения подногтевой меланомы. В этом обзоре сделан вывод, что операция по удалению на месте меланом и меланом более низкой степени злокачественности является разумным вариантом.Это переводится как иссечение до надкостницы или паратенона. Другие более глубокие меланомы более высокой степени злокачественности могут подвергаться ампутации на более дистальном уровне (межфаланговый сустав), чем рекомендовано Дасом Гуптой. Однако, несмотря на обнадеживающие доказательства того, что хирурги рассматривают менее агрессивные варианты лечения, качество данных низкое, отсутствуют рандомизированные контролируемые исследования и сбор данных в основном ретроспективный. Метод хирургического удаления остается спорным и должен оцениваться в индивидуальном порядке.
Эти рекомендации должны помочь определить удаление подногтевой меланомы, но, возможно, потребуется скорректировать их, чтобы обеспечить наиболее функциональный результат для пациента.
Пациентам с клинически пальпируемыми узлами следует предложить лимфодиссекцию. Согласно национальным рекомендациям Соединенного Королевства, всем пациентам с меланомой глубиной от 1 до 4 мм следует предлагать биопсию дозорных лимфатических узлов. Тем, у кого лимфоузел положительный на микрометастаз, следует предложить завершенную лимфодиссекцию.
Радиационная онкология
Лучевая терапия имеет ограниченное применение при меланоме и должна применяться только в определенных обстоятельствах. Он предназначен для использования в бассейне лимфатических узлов при постлимфаденэктомии в случаях, когда возникла объемная лимфаденопатия или экстракапсулярное заболевание. Также рекомендуется для лечения метастазов в мозг.
Медицинская онкология
Иммунотерапия — это вариант, который можно обсудить с пациентами с метастатическим заболеванием и предложить онкологам.
Стадия
Подногтевая меланома определяется с использованием системы стадирования и классификации AJCC. Стадия метастазирования узла опухоли (TNM) используется так же, как и для других злокачественных меланом.
Прогноз
В некоторых публикациях сообщается о худшем прогнозе для подногтевой меланомы по сравнению с меланомой кожи. Вероятно, это связано с поздним проявлением заболевания. Таким образом, прогноз, скорее всего, будет таким же, как и при кожной злокачественной меланоме.
Американское онкологическое общество недавно опубликовало актуальную прогностическую статистику:
Стадия IA: 5-летняя выживаемость составляет около 97%.10-летняя выживаемость составляет около 95%.
Стадия IB: 5-летняя выживаемость составляет около 92%. 10-летняя выживаемость составляет около 86%.
Стадия IIA: 5-летняя выживаемость составляет около 81%. 10-летняя выживаемость составляет около 67%.
Стадия IIB: 5-летняя выживаемость составляет около 70%. 10-летняя выживаемость составляет около 57%.
Стадия IIC: 5-летняя выживаемость составляет около 53%. 10-летняя выживаемость составляет около 40%.
Стадия IIIA: 5-летняя выживаемость составляет около 78%.10-летняя выживаемость составляет около 68%.
Стадия IIIB: 5-летняя выживаемость составляет около 59%. 10-летняя выживаемость составляет около 43%.
Стадия IIIC: 5-летняя выживаемость составляет около 40%. 10-летняя выживаемость составляет около 24%.
Стадия IV: 5-летняя выживаемость составляет от 15% до 20%. 10-летняя выживаемость составляет от 10% до 15%. Перспектива лучше, если распространение происходит только на отдаленные участки кожи или удаленные лимфатические узлы, а не на другие органы, и если уровень лактатдегидрогеназы (ЛДГ) в крови нормальный.
Осложнения
Дистрофия ногтей может возникнуть после операции.
Косметическая деформация наблюдается у всех пациентов.
Послеоперационный и реабилитационный уход
Пациенты, которые отказываются от биопсии, должны находиться под тщательным наблюдением.
Сдерживание и обучение пациентов
Пациенты должны понимать, что подногтевая меланома не связана с пребыванием на солнце. В дальнейшем им следует соблюдать правила гигиены рук и ног, что может принести определенную пользу.Им также следует осмотреть ногти и ногтевые ложа на предмет признаков рецидива или других новых поражений.
Жемчуг и другие проблемы
Ключевые моменты, которые следует помнить при подногтевой меланоме:
Гистопатологический процесс аналогичен кожной злокачественной меланоме.
Некоторые исследования показывают, что она более агрессивна, чем кожная злокачественная меланома, но это, вероятно, связано с поздним проявлением.
Диагноз следует диагностировать с помощью иссечения или разрезной биопсии.
Граница иссечения определяется глубиной опухоли и может привести к ампутации части или всего пальца.
Улучшение результатов медицинской бригады
Подногтевая меланома чаще всего встречается у лиц не европеоидной расы, причем как мужчины, так и женщины имеют равный риск. Как и другие формы меланомы, подногтевая меланома также может распространяться на другие части тела и является летальной. Ключ к диагностике и раннему лечению — осведомленность. Все медицинские работники, в том числе медсестры, должны регулярно осматривать ногти и поддерживать высокий индекс подозрений на любые пигментные поражения на ногтях.Единственный способ снизить высокую смертность — это как можно скорее обратиться к дерматологу на биопсию. Кроме того, медсестра должна обучать пациентов проверять их кожу и ногти на предмет необычных изменений. Наконец, и медсестра, и фармацевт должны информировать общественность об использовании солнцезащитного крема при выходе на улицу и использовании защитной одежды при выходе на улицу. Солнцезащитные очки также рекомендуются, поскольку ультрафиолетовые лучи солнца могут повредить клетки сетчатки. [14] [15] [Уровень 5]
Исходы
Для ранних поражений результаты хорошие, но для запущенных поражений результаты плохие.На выживаемость без болезней не влияет тип операции на ногте. Чем раньше будет поставлен диагноз, тем выше выживаемость. [16] [17] [Уровень 5]
Повышение квалификации / Вопросы для повторения
Рисунок
подногтевая меланома среднего пальца. Предоставлено С. Бхимджи, MD
Ссылки
- 1.
- Нуньес Л.Ф., Квинтелла Мендес Г.Л., Койфман Р.Дж. Акральная меланома: ретроспективная когорта из Бразильского национального института рака (INCA). Melanoma Res.Октябрь 2018; 28 (5): 458-464. [PubMed: 30020197]
- 2.
- Оздемир Ф., Эррико М.А., Яман Б., Караарслан И. Акральная лентигинозная меланома у населения Турции и новый дерматоскопический ключ к диагностике. Концепция Dermatol Pract. 2018 Апрель; 8 (2): 140-148. [Бесплатная статья PMC: PMC5955083] [PubMed: 29785333]
- 3.
- Nakamura Y. [II. Диагностика и лечение меланомы ногтевого аппарата (подногтевой). Ган То Кагаку Риохо. 2018 Апрель; 45 (4): 619-621. [PubMed: 29650816]
- 4.
- Boespflug A, Debarbieux S, Depaepe L, Chouvet B, Maucort-Boulch D, Dalle S, Balme B, Thomas L. Ассоциация подногтевой меланомы и подногтевой плоскоклеточной карциномы: серия случаев. J Am Acad Dermatol. 2018 апр; 78 (4): 760-768. [PubMed: 28947295]
- 5.
- Декер А., Коннолли К.Л., Ли Э.Х., Бусам К.Дж., Нехал К.С. Частота подногтевой меланомы при продольной меланонихии: опыт одного центра. Dermatol Surg. 2017 июн; 43 (6): 798-804. [PubMed: 28296790]
- 6.
- Ингканинанда П., Висессири Ю., Рутнин С. Клинико-патологические особенности и прогностические факторы злокачественной меланомы: ретроспективный анализ тайских пациентов в больнице Раматибоди. J Med Assoc Thai. 2015 август; 98 (8): 820-7. [PubMed: 26437541]
- 7.
- Talavera-Belmonte A, Bonfill-Ortí M, Martínez-Molina L, Fornons-Servent R, Bauer-Alonso A, Ferreres-Riera JR, Marcoval J. Подногтевая меланома: описательное исследование из 34 больных. Actas Dermosifiliogr. 2018 ноя; 109 (9): 801-806.[PubMed: 30082026]
- 8.
- Ohn J, Jo G, Cho Y, Sheu SL, Cho KH, Mun JH. Оценка модели прогнозной оценки для дерматоскопии подногтевой меланомы in situ. JAMA Dermatol. 1 августа 2018 г .; 154 (8): 890-896. [Бесплатная статья PMC: PMC6143019] [PubMed: 29926108]
- 9.
- Wollina U, Nenoff P, Haroske G, Haenssle HA. Диагностика и лечение заболеваний ногтей. Dtsch Arztebl Int. 2016 25 июля; 113 (29-30): 509-18. [Бесплатная статья PMC: PMC5527843] [PubMed: 27545710]
- 10.
- Sinno S, Wilson S, Billig J, Shapiro R, Choi M. Первичная меланома руки: алгоритмический подход к хирургическому лечению. J Plast Surg Hand Surg. 2015; 49 (6): 339-45. [PubMed: 26051472]
- 11.
- Кокран А.М., Бьюкенен П.Дж., Буэно Р.А., Ноймейстер М.В. Подногтевая меланома: обзор современного лечения. Plast Reconstr Surg. 2014 август; 134 (2): 259-273. [PubMed: 25068326]
- 12.
- Тан КБ, Монкрифф М., Томпсон Дж.Ф., Маккарти С.В., Шоу Х.М., Куинн М.Дж., Ли LX, Кротти К.А., Стретч-младший, Сколайер Р.А.Подногтевая меланома: исследование 124 случаев, в котором подчеркиваются особенности ранних поражений, потенциальные ошибки в диагностике и рекомендации по гистологической отчетности. Am J Surg Pathol. 2007 декабрь; 31 (12): 1902-12. [PubMed: 18043047]
- 13.
- Левит Е.К., Каген М.Х., Шер Р.К., Гроссман М., Альтман Э. Правило ABC для клинического обнаружения подногтевой меланомы. J Am Acad Dermatol. 2000 Февраль; 42 (2 Пет 1): 269-74. [PubMed: 10642684]
- 14.
- Чемберлен А., Нг Дж. Меланома кожи — атипичные варианты и проявления.Врач Ост Фам. 2009 Июль; 38 (7): 476-82. [PubMed: 19575065]
- 15.
- Паври С.Н., Клун Дж., Ариян С., Нараян Д. Злокачественная меланома: помимо основ. Plast Reconstr Surg. 2016 Август; 138 (2): 330e-340e. [PubMed: 27465194]
- 16.
- Möhrle M, Lichte V, Breuninger H. [Оперативная терапия акральной меланомы]. Hautarzt. 2011 Май; 62 (5): 362-7. [PubMed: 21468730]
- 17.
- Sureda N, Phan A, Poulalhon N, Balme B, Dalle S, Thomas L. Консервативное хирургическое лечение подногтевой (матриксной) меланомы: отчет о семи случаях и обзор литературы.Br J Dermatol. 2011 Октябрь; 165 (4): 852-8. [PubMed: 21812768]
Жена размышляет о шокирующем диагнозе мужа | Онкологический центр Андерсона
Моему мужу Стиву поставили диагноз меланома IV стадии в январе 2012 года в возрасте 34 лет.
У нас две дочери 2 и 10 лет. Он только начал работать дома, и наша жизнь, казалось, шла гладко.
У меня были незначительные проблемы со здоровьем, которые мешали мне работать, а новая работа Стива позволила мне оставаться дома и сосредоточиться на том, чтобы поправиться.
Однажды в декабре 2011 года Стив попросил меня почувствовать странную шишку на его шее. Она находилась прямо над его правой ключицей и распухла примерно до размера яйца.
Я немедленно начал рыскать по Интернету, пытаясь понять, что происходит. Через несколько минут я определил, что это надключичный лимфатический узел.
Все, что я читал о правом надключичном лимфатическом узле, указывало на рак или очень серьезную инфекцию.
Стив только что простудился, так что я надеялся, что это как-то связано с этим.Через несколько дней он не упал. В этот момент он тоже начал волноваться, поэтому мы решили пойти в скорую.
Они сделали анализ крови и рентген головы / шеи и сказали, что все в порядке. Они попросили нас вызвать нашего специалиста по уху, носу и горлу, если это не пройдет через неделю.
Через неделю лимфатический узел все еще опух. Мы записались на прием к нашему ЛОРу, который сразу направил нас к патологу на биопсию. Патолог выполнил тонкую пункционную аспирацию лимфатического узла, и мы ждали результатов около 10 дней.
Шокирующие результаты
Метастатическая меланома. Какие? Как у Стива может быть рак? Как ему от этого избавиться?
Мы пришли домой и начали читать о меланоме в Интернете. То, что мы прочитали, было шокирующим. Мы оба плакали.
Средняя продолжительность жизни пациента с меланомой IV стадии составляет 6–22 месяца. Как может внешне здоровый 34-летний мужчина внезапно умереть? Это просто не имело смысла.
Мы должны были собраться и приготовиться бороться с этим и победить это.
Наш ЛОР направил нас к онкологу общего профиля, доктору Эми Хассан, в Региональный онкологический центр доктора медицины Андерсона в районе залива. Нам пришлось ждать около пяти дней, чтобы попасть на эту встречу, но как только мы приехали, дела пошли быстро.
Доктор Хасан отправил Стива в кампус Техасского медицинского центра доктора медицины Андерсона для проведения МРТ, компьютерной томографии и ПЭТ. Мы получили результаты через несколько дней. В январе 2012 года нам поставили официальный диагноз: метастатическая меланома IV стадии.
МРТ было четким, меланома распространилась на лимфатический узел Стива, надпочечник и нижнюю левую долю его легкого.
Затем доктор Хассан направил нас к одному из специалистов по меланоме в главном кампусе доктора медицины Андерсона, доктору Кевину Киму.
После встречи с доктором Ким мы почувствовали себя немного лучше.
Начало лечения
Он был очень открытым и честным в отношении того, что происходило, и не пытался приукрашивать ситуацию и заставлять нас думать, что все будет хорошо.
Он был очень информативен, объясняя варианты лечения Стива. Он сообщил нам, что собирается сделать все, что в его силах, чтобы сохранить ему жизнь, чтобы он мог видеть, как его дочери выпускаются и выходят замуж.
Доктор Ким хотел как можно скорее направить Стива на биохимиотерапию. На следующей неделе Стив был госпитализирован, чтобы начать свой первый курс лечения.
Так началось наше путешествие с MD Anderson. Следуйте за нами на martinfamilyjourney.blogspot.com.
Меланома с неизвестной первичной — некожная меланома
Abstract
Хотя у подавляющего большинства меланом есть известная первичная локализация, примерно 3,2% всех меланом находятся в отдаленных местах, где первичная локализация неизвестна.Меланома неизвестной первичной формы чаще всего проявляется в лимфатических узлах, затем подкожных участках и, наконец, во внутренних органах. Были предложены различные гипотезы относительно происхождения меланомы неизвестной первичной опухоли, включая спонтанную регрессию первичной опухоли и наличие эктопических меланоцитов в лимфатических узлах и висцеральных органах. Меланома неизвестной первичной формы менее изучена по сравнению с меланомой известной первичной, но ее клинические, молекулярные и генетические характеристики были недавно выяснены.В частности, меланома неизвестной первичной формы чаще встречается у мужчин четвертого и пятого десятилетий жизни и имеет такую же генетическую и молекулярную подпись, что и кожные меланомы, возникающие на коже, периодически подвергающейся воздействию солнца, включая спину и верхнюю часть ног. Кроме того, прогноз для этих пациентов также был уточнен, и пациенты с меланомой неизвестной первичной формы улучшили выживаемость по сравнению с пациентами подобранной по стадии с меланомой известной первичной. В этой главе рассматриваются последние достижения в понимании меланомы с неизвестной первичной локализацией, выделяются ее генетические и молекулярные характеристики, эпидемиология, прогноз и лечение, а также ее связь с меланомой известной первичной локализации.
Ключевые слова:
Эпидемиология, Меланома известной первичной, Меланома неизвестной первичной, Метастатическая меланома, ПрогнозВВЕДЕНИЕ
Более 97% всех меланом диагностируются с известной первичной локализацией, чаще всего поражающей кожу (1 ). Реже меланома может присутствовать в глазу или на слизистых оболочках (1). В редких случаях меланома диагностируется без очевидного первичного очага и называется меланомой неизвестного первичного очага (MUP). В 1963 году Дас Гупта первоначально определил MUP как меланому, обнаруженную в подкожной клетчатке, лимфатических узлах (ЛУ) или внутренних органах без первичного участка кожи, глаз или слизистой оболочки (2).
Известная первичная меланома (MKP) обычно ошибочно классифицируется как MUP. Эта ошибка возникает из-за отсутствия знаний об истинном первичном локализации меланомы, что может быть результатом неполного физического обследования всех поверхностей кожи, глаз и слизистых оболочек или из-за отсутствия в анамнезе ранее леченной или регрессивной меланомы. Учитывая изначально проблематичный характер точного определения MUP в клинической практике, Дас Гупта также описал четыре критерия исключения, которые должны были помочь в характеристике MUP () (2).Если какой-либо из этих критериев исключения соблюдался, Дас Гупта предложил классифицировать пациентов как имеющих МКР, а не МУП (2).
ТАБЛИЦА 1
Критерии исключения меланомы неизвестной первичной, первоначально предложенные Дасом Гуптой (2).
Несмотря на эти предложенные критерии исключения, пациенты с MUP, описанные в литературе на сегодняшний день, были неоднородными, с широкими вариациями в том, как определяется MUP, и в интерпретации критериев исключения. Фактически, в недавнем систематическом обзоре MUP Kamposioras et al.сообщили, что только 16% рецензируемых статей и рефератов использовали исходные критерии Даса Гупты для характеристики MUP (3). Чаще всего исследования различаются по полноте физического обследования, которое требуется перед постановкой диагноза MUP, включая различную степень кожного, орального, окулярного, отоларингологического, урогенитального и проктоскопического обследования (3). В частности, в отношении поверхностей слизистой оболочки, нет единого мнения о том, насколько тщательным должно быть обследование участков слизистой оболочки перед установлением диагноза MUP (3).
ГИПОТЕЗЫ ОТНОСИТЕЛЬНО ПРОИСХОЖДЕНИЯ MUP
Начиная с первоначального определения, были выдвинуты различные гипотезы, чтобы помочь объяснить биологический феномен MUP. Метастатическая меланома теоретически может развиваться синхронно с субклинической или иначе нераспознанной меланомой кожи, глаза или слизистой оболочки (2, 4). Однако это менее вероятное объяснение MUP, если время последующего наблюдения адекватно, поскольку известное первичное заболевание, вероятно, заявит о себе к тому времени, когда разовьется метастатическое заболевание.
Преобладающая гипотеза MUP включает спонтанную регрессию меланомы с известной первичной локализации. Теория регрессии, впервые предложенная Smith и Stehlin в 1965 году, связывает исчезновение первичной меланомы со спонтанной регрессией после метастазирования (5). Частичная или полная спонтанная регрессия меланомы из известного первичного очага хорошо документирована в литературе, и на меланому приходится 11% всех случаев спонтанной регрессии опухоли (6–9).Однако, в то время как частичная регрессия первичной меланомы довольно распространена и, по оценкам, встречается в 9–46% всех меланом, полная регрессия очень редка и, по оценкам, встречается только в 0,22–0,27% всех меланом (6, 10–10). 13). Исследования, сообщающие о регрессии конкретно у пациентов с MUP, показывают, что примерно 12,4% случаев связаны с регрессом до или после диагностики MUP (6, 11–13).
Спонтанный регресс меланомы, вероятно, является иммуноопосредованным, включая как клеточно-опосредованные, так и гуморальные иммунные механизмы (10).Регрессирующие меланомы характеризуются увеличением количества инфильтрирующих опухоль лимфоцитов, что также дает благоприятный прогноз (14, 15). Иммунные ответы на антигены, связанные с меланомой, также опосредуются цитотоксическими Т-лимфоцитами (16). Кроме того, существует высокая распространенность специфических антител к меланоме в сыворотке пациентов с MUP, и различные гуморальные иммунные механизмы, включая прикрепление антител к клеточным мембранам, цитотоксичность и разрушение опухоли, были описаны с культивированными клетками меланомы in vitro. (12, 17–22).
Альтернативно, MUP можно также объяснить присутствием эктопических меланоцитов или дифференцировкой меланоцитов из уже существующих плюрипотентных стволовых клеток в подкожной ткани, LNs или висцеральных органах (4). Меланоциты происходят из нервного гребня и мигрируют по дорсолатеральным путям во время эмбриогенеза, чтобы достичь кожи и волосяных фолликулов (23). Меланоциты также мигрируют во внутреннее ухо, лептоменинги и увеальный тракт глаза, который включает сосудистую оболочку, цилиарное тело и радужную оболочку (23).Иногда меланоциты также обнаруживаются на других участках слизистой оболочки, включая конъюнктиву, слизистую оболочку носоглотки, пищевод и слизистую оболочку прямой кишки (23). Что касается LN, то сообщалось о скоплениях доброкачественных клеток невуса и голубых невусах в LN и других тканях, и, что интересно, сообщалось о меланоме, возникающей из эктопических меланоцитов внутри LN (24-27). Таким образом, меланома, обнаруженная в LN, может происходить из злокачественной дегенерации меланоцитов, происходящих из нервного гребня, которые мигрировали и задерживались в LN, или, альтернативно, из клеток доброкачественного невуса, которые мигрировали из кожи в дренирующие LN.
Кроме того, некоторые исследователи задаются вопросом, действительно ли сообщения о MUP, диагностированном в висцеральных органах, представляют собой первичные меланомы, возникающие в уникальных анатомических местах. Например, желудочно-кишечный тракт является частым местом метастазирования кожной меланомы, а также наиболее широко описываемым внутренним участком для MUP (3, 28). Было высказано предположение, что случаи MUP желудочно-кишечного тракта могут фактически представлять случаи первичной меланомы, происходящей из меланобластических клеток нервного гребня (28).Известно, что меланобластные клетки мигрируют в тонкую кишку, преимущественно в подвздошную кишку, через омфаломезентериальный канал (28). Эти меланобластические клетки дифференцируются в эктопические меланоциты желудочно-кишечного тракта, которые теоретически в редких случаях могут образовывать первичные меланомы желудочно-кишечного тракта (28). Наконец, в литературе существует путаница в отношении присутствия MUP в надпочечниках. Мозговое вещество надпочечников содержит нейроэндокринные клетки, происходящие из нервного гребня, и некоторые считают, что MUP, диагностированный в надпочечнике, вместо этого следует называть первичной меланотической злокачественной феохромоцитомой надпочечников (29).
ГЕНЕТИКА
Генетические профили кожных, акральных, глазных и слизистых меланом значительно различаются. Недавние исследования изучили генетический профиль MUP (30). В частности, MUP имеет много общих генетических и молекулярных признаков меланомы, возникающей из-за периодически подвергающихся воздействию солнца участков кожи, включая спину и верхнюю часть ног (31–33). Анализ 102 пациентов с MUP после терапевтической лимфаденэктомии показал, что мутации BRAF и NRAS произошли в 53 и 14% образцов MUP, соответственно (31).Следует отметить, что мутации BRAF V600E скомпрометировали 93% всех мутаций BRAF в этой когорте MUP, и мутации c-KIT не были идентифицированы (31). Таким образом, генотип MUP наиболее близок к генотипу меланомы кожи, особенно к поверхностным распространяющимся и узловым гистологическим подтипам, возникающим из периодически поврежденной солнцем кожи (33, 34). Эта генетическая подпись отличается от меланомы кожи, возникающей из хронически поврежденной солнцем кожи, акральной кожи и участков слизистой оболочки, которые обычно обогащены мутациями c-KIT (34).В отдельном анализе 39 пациентов с MUP мутации в промоторе TERT были обнаружены чаще при MUP, чем при меланоме слизистой оболочки (66,7% против 13,2%, соответственно) (35). Наличие мутаций промотора TERT в опухолях MUP коррелировало с более высоким процентом мутаций BRAF и NRAS, что привело к гипотезе о том, что мутации промотора TERT могут действовать как мутации-драйверы в MUP (35).
ТАБЛИЦА 2
Общие мутации в меланоме неизвестной первичной по сравнению с меланомой известной первичной.
ЗАБОЛЕВАЕМОСТЬ И ДЕМОГРАФИЯ
Вероятно, связанная с присущей трудностью определения MUP, частота MUP широко сообщается, варьируя от 1,2% до 31% (36–38). Недавно большой систематический обзор прояснил истинную заболеваемость MUP и сообщил об общей заболеваемости 3,2%, которая оставалась стабильной, когда дети и подростки были исключены из анализа (3). Широкий диапазон заболеваемости, о котором ранее сообщалось в литературе, также можно частично объяснить улучшением технологии медицинской визуализации, которая может привести к более точной идентификации первичной опухоли (3).В приведенном выше систематическом обзоре заболеваемость MUP до эры современной компьютерной томографии (3) в 1980 г. составляла 5,1% по сравнению с 2,7% после 1980 г. (3).
Пик заболеваемости MUP приходится на четвертое и пятое десятилетия жизни, что сопоставимо с меланомой кожи, но раньше, чем меланома слизистой оболочки и глаза (1, 39). Более молодой возраст пика заболеваемости MUP может быть связан с устойчивыми иммунными ответами более молодых пациентов, что приводит к более высокой скорости регрессии первичного сайта (3). Более того, MUP встречается в два раза чаще у мужчин, чем у женщин, и это было связано с эпидемиологическими факторами, связанными с повышенной вероятностью регрессии первичной локализации (3).Например, мужчины могут с большей вероятностью игнорировать первичную кожную меланому до тех пор, пока она полностью не регрессирует и позже не перейдет в метастатическое заболевание, а мужчины также более склонны к развитию меланомы в анатомических участках, где регресс может быть более вероятным, включая спину. и кожа головы (3).
МЕТАСТАТИЧЕСКИЕ УЧАСТКИ
MUP чаще всего диагностируется в LN (40–60% всех случаев) и, как сообщается, вовлекает подмышечные, шейные, паховые и околоушные LN в 52.2, 32.7, 28,3 и 2,6% случаев соответственно (3, 13, 40). У мужчин MUP чаще всего проявляется в подмышечных и шейных ЛУ, а у женщин — в паховых ЛУ (3). Более высокая частота поражения паховых лимфатических узлов у женщин по сравнению с мужчинами объясняется более высокой частотой развития меланомы нижних конечностей и аногенитальной меланомы у женщин (4).
После LN, MUP чаще всего диагностируется в подкожных тканях (примерно в 30% случаев) и реже всего диагностируется в висцеральных органах (примерно в 20% случаев) (3, 13).В недавнем систематическом обзоре MUP, 5,1% пациентов имели подкожное поражение, 4,9% — одно или несколько висцеральных участков и 0,7% — костные отложения (3). При MUP сообщается о множестве внутренних органов, включая мозг, околоушную железу, сердце, средостение, легкие, грудь, печень, общий желчный проток, тонкий и толстый кишечник, почки, надпочечники, простату, кости, костный мозг и мышцы. (29, 41–65). Как и ожидалось, в литературе описаны различные клинические проявления висцерального заболевания в зависимости от пораженного органа (46, 49, 59, 66–72).MUP также может проявляться как паранеопластический синдром, описываемый как ретинопатия, системный васкулит, воспалительная демиелинизирующая полинейропатия, диффузная витилиго-подобная депигментация и синдром Горхэма-Стаута или исчезающая болезнь костей (73–78). Витилиго-подобная депигментация, по-видимому, является довольно частым проявлением широко распространенного метастатического заболевания и может предшествовать обнаружению MUP на срок до 18 месяцев (76, 79, 80).
ТАБЛИЦА 3
Различные клинические проявления меланомы неизвестной первичной (46).
Следует выделить несколько особых соображений, касающихся поражения внутренних органов. Во-первых, первичная первичная меланома может стать клинически очевидной после постановки диагноза MUP. Например, Kumar et al. сообщили о случае 56-летней женщины с MUP, диагностированной в левой подмышечной ЛУ, у которой через 18 месяцев после первоначального диагноза MUP была обнаружена первичная кожная меланома левого пальца (81). Во-вторых, MUP может иметь различные гистологические проявления, которые часто могут усложнять патологический диагноз и подчеркивают важность иммуногистохимии в постановке диагноза MUP.MUP был описан как новообразование из перстневых клеток с многочисленными промежуточными филаментами, которое распознавалось как новообразование меланоцитов только при положительном окрашивании на виментин, S-100 и HMB-45 (82). Аналогичным образом Adler et al. описали случай ангиоматоидной меланомы, имитирующей сосудистую злокачественную опухоль, гистологически охарактеризованную как опухоль из веретенообразных клеток с многочисленными кавернозными, заполненными эритроцитами пространствами и лишь скудной пигментацией меланина (83).
СТАДИЯ И ПРОГНОСТИЧЕСКИЕ ФАКТОРЫ
Прогностические факторы пациентов с MUP аналогичны таковым для MKP с той же клинической стадией на момент обращения (84–86).Однако до недавнего времени не существовало единых руководящих принципов по стадированию MUP (8, 87, 88). В 2009 году система определения стадии меланомы Американского объединенного комитета по раку (AJCC) классифицировала MUP как заболевание III стадии, если при первичном обращении присутствовало поражение LN или подкожной клетчатки, и как заболевание стадии IV при поражении внутренних органов (89). Белок S100 сыворотки и позитронно-эмиссионная томография (ПЭТ) рекомендуются для определения исходного уровня пациентов с MUP (90). В одном исследовании уровень сывороточного белка S100 был повышен у 35% пациентов с MUP, а сканирование с помощью ПЭТ выявило скрытые отдаленные метастазы у 86% пациентов с MUP (90).Кроме того, отдаленные метастазы были связаны со значительно более высокими уровнями белков S100 в сыворотке, что позволяет предположить, что белок S100 в сыворотке может быть чувствительным и специфическим маркером для выявления скрытого отдаленного метастатического заболевания у пациентов с MUP (90).
Подобно MKP, возраст пациента, стадия AJCC, уровень лактатдегидрогеназы и количество метастазов на момент постановки диагноза являются независимыми прогностическими факторами MUP (91). Кроме того, в многофакторном анализе, стратифицированном по стадии AJCC, транзитные метастазы и количество вовлеченных LN являются независимыми прогностическими факторами для III стадии заболевания, а возраст и уровень лактатдегидрогеназы на момент диагностики являются независимыми прогностическими факторами для IV стадии (91).Дополнительные положительные прогностические факторы для MUP включают свидетельство регрессии опухоли, меньшее количество вовлеченных LN и быстрое хирургическое лечение в течение 3 месяцев (3, 86, 91–93). Более того, четыре исследования сообщили о лучшем прогнозе для более молодых пациентов, но влияние пола на прогноз еще предстоит полностью выяснить (3, 36, 91, 94, 95). Отрицательные прогностические факторы включают поражение шейных ЛУ, экстракапсулярное расширение и наличие транзитных метастазов (86, 88, 91, 96, 97). В конечном итоге, поражение LN было определено как наиболее важный прогностический фактор при MUP (97).В частности, учитывая только стадию заболевания IV, повышенное количество метастазов и лактатдегидрогеназа при поступлении были связаны со значительно худшими результатами (91).
Что касается мутационного статуса, то наличие мутаций BRAS, NRAS и TERT-промотора, по-видимому, не имеет значительного прогностического влияния, поскольку нет корреляции между мутационным статусом и общей выживаемостью (OS) для пациентов с MUP (31, 33) . Интересно, что пациенты с MUP с витилиго могли улучшить выживаемость (13, 98).Например, витилиго было диагностировано у 5 из 88 пациентов с MUP в одной когорте, и наличие витилиго было связано с благоприятным прогнозом (13). Другое исследование описало длительную выживаемость, связанную с развитием витилиго, через 6 лет после диагноза MUP в подмышечных лимфатических узлах (99). В этом случае рецидива меланомы через 10 лет после хирургической резекции пораженных ЛУ не было (99).
ВЫЖИВАНИЕ
Медиана OS колеблется от 24 до 127 месяцев для пациентов с MUP с заболеванием LN (стадия III AJCC), с 5- и 10-летним OS в диапазоне от 28.От 6 до 75,6% и от 18,8 до 62,9% соответственно (3, 39). ОС на стадии III MUP значительно лучше, чем у пациентов с MUP с висцеральной стадией (стадия IV AJCC), при этом медиана OS составляет от 3 до 13 месяцев, 5-летняя OS составляет от 5,9 до 18%, а 10-летние выживающие , 39). В систематическом обзоре MUP семь исследований продемонстрировали значительно лучший прогноз для узлового MUP по сравнению с подкожным или висцеральным MUP (1, 8, 11, 91, 95, 100, 101). Что касается влияния хирургического лечения на выживаемость, быстрое радикальное рассечение LN шеи привело к повышению выживаемости в трех исследованиях, тогда как модифицированное радикальное рассечение LN шеи привело к повышению выживаемости только в одном исследовании (1, 8, 102, 103).Однако прогностическое преимущество модифицированной и радикальной диссекции ЛУ шеи не может быть окончательно определено в систематическом обзоре (3). Подобно III стадии MKP, безоперационное лечение MUP стадии III связано с худшей выживаемостью по сравнению с хирургическим лечением (3). Некоторые исследователи предполагают, что хирургическое вмешательство не только снижает общую опухолевую нагрузку, но также снижает степень иммуносупрессии, позволяя развиваться противоопухолевому иммунитету (3).
Выживаемость MUP по сравнению с пациентами MKP
Несколько исследований, в которых пытались сравнить различия в выживаемости между MUP и пациентами MKP с использованием сопоставимых пациентов и исторического контроля, показали смешанные результаты.Еще в 1998 г. Vijuk и Coates сообщили о средней выживаемости 233 дня для пациентов с MUP по сравнению с 176 днями для пациентов с MKP (104). Аналогичным образом Prens et al. изучили результаты пациентов с MUP после терапевтического рассечения LN шеи и обнаружили тенденцию к увеличению выживаемости в MUP по сравнению с пациентами с MUP с 5-летним OS 40 и 27%, соответственно (105). Совсем недавно Weide et al. также сообщили об улучшении ОВ у пациентов с MUP по сравнению с пациентами MKP с поражением LN (медиана OS 65 месяцев против 24 месяцев, соответственно) (96, 97).Что касается болезни IV стадии, ретроспективный анализ 534 пациентов с MUP стадии IV и средний период наблюдения 10,4 месяца показал, что пациенты MUP имели такую же выживаемость, как кожная меланома и увеальная меланома с момента первого отдаленного метастазирования, но значительно лучшую выживаемость, чем меланома слизистой оболочки (106).
Статистически значимая разница в выживаемости между пациентами с MUP и MKP была продемонстрирована лишь в нескольких опубликованных исследованиях (3). Ли и др. сообщили о значительно более высокой 5-летней выживаемости для пациентов с MUP по сравнению с пациентами с MKP при сопоставлении по метастазам в лимфоузлы, месту метастазирования и количеству участков метастазирования (36, 39).Сопоставление пациентов со стадией III на основании четырех дополнительных ковариат, включая возраст, пол, бремя узловой опухоли и десятилетие постановки диагноза, также выявило значительно более высокую медианную ОС для MUP по сравнению с пациентами MKP (164 месяца против 34 месяцев, соответственно) (39) .
Пытаясь уточнить прогноз MUP по сравнению с пациентами MKP, Bae et al. недавно провели метаанализ всех исследований, в которых сообщалось о выживаемости на сегодняшний день, и сообщили о лучшей общей выживаемости у пациентов с MUP стадии III по сравнению с пациентами MKP (отношение рисков 0.83, 95% доверительный интервал 0,73–0,96, P = 0,01) и пациенты с MUP стадии IV по сравнению с пациентами MKP (отношение рисков 0,85, 95% доверительный интервал 0,75–0,96, P = 0,08) (107). Анализ подгрупп также показал, что у пациентов с MUP с узловым поражением только улучшилась общая выживаемость (отношение рисков 0,82, 95% ДИ 0,71–0,95) и выживаемость без болезни по сравнению с пациентами MKP (отношение рисков 0,84, 95% ДИ 0,70–1,00) (107) . Повышенная выживаемость пациентов со стадией III и IV MUP по сравнению с пациентами MKP особенно поразительна, учитывая, что систематическая ошибка заблаговременности по своей сути должна способствовать увеличению выживаемости пациентов с MKP, поскольку наличие известного первичного заболевания, вероятно, приведет к более ранней диагностике каждого заболевания сцена.
ДИАГНОСТИКА
Тщательное обследование, включая офтальмологическое и аногенитальное обследования, требуется, когда меланома диагностируется в подкожно-жировой клетчатке, ЛУ или висцеральных органах без очевидного первичного источника. Тем не менее, точный тип обследования, который рекомендуется пациентам с MUP после полного физического обследования, является спорным (). В одном исследовании 103 пациентов с MUP Tos et al. обнаружили, что 84% пациентов были обследованы офтальмологом, 82% — оториноларингологом и 89% — гинекологом (108).Более того, 92% пациентов с MUP выполняли дополнительную визуализацию желудочно-кишечного тракта, включая ректороманоскопию и проктоскопию (108). Из дополнительных направлений и оценок, выполненных в этом конкретном исследовании, единственным обнаруженным первичным очагом была недиагностированная меланома хориоидеи (108). Основываясь на этих результатах, эта группа рекомендовала подробный анамнез, физикальное обследование, гистопатологический обзор и КТ и / или ПЭТ для точного определения стадии для всех новых пациентов с MUP, но предположила, что дополнительные направления к специалистам и специализированные обследования могут быть излишними (108).
Рисунок 1
Обследование впервые выявленной меланомы неизвестного первичного происхождения.
Аналогичным образом, всемирный опрос 119 поставщиков в 47 странах проанализировал клинические и лабораторные обследования, необходимые для пациентов с MUP после тщательного сбора анамнеза и физического обследования (109). Половина всех респондентов специально оценивалась на наличие витилиго, которое может помочь объяснить регресс первичного очага (109). Три четверти всех респондентов применяли те же протоколы для пациентов с MUP, что и пациенты с MKP, соответствующие стадии AJCC (109).Кроме того, все респонденты спрашивали об истории предыдущих иссечений кожи, и 81% просмотрели гистопатологические слайды из предыдущих биопсий (109). В частности, очень важен гистопатологический обзор опытным патологом, поскольку MUP может имитировать другие новообразования веретенообразных клеток. Например, MUP околоушной железы имитировал саркому встречных дендритных клеток и в конечном итоге потребовал иммуногистохимического окрашивания для точного определения меланоцитарного происхождения опухоли (110). В другом случае новообразования в корнях легких и средостения изначально с большой вероятностью указывали на первичный рак легкого рентгенологически, но в конечном итоге после гистологического анализа были обнаружены S100-отрицательные MUP (111).
Кроме того, очень важно долгосрочное наблюдение, так как оккультная первичная клиническая картина может стать клинически очевидной через 5 лет после первоначального диагноза MUP. В одном сообщении о MUP, диагностированном в печени и подвергнутом лечению химиотерапией и лучевой терапией, наиболее вероятная первичная меланома слизистой оболочки носоглотки стала клинически очевидной только через 6 лет после первоначального диагноза MUP из-за нового носового кровотечения (112). В другом сообщении о случае MUP, диагностированном в тонкой кишке, наиболее вероятная первичная болезнь стала клинически очевидной на коже черепа через 15 лет после первоначального диагноза MUP (113).Эти отсроченные представления первичного очага могли быть результатом неполного физического обследования во время первоначального диагноза MUP, или они могли быть связаны с изменениями в иммунных ответах пациентов, что привело к росту первичной опухоли до такой степени, что он стал клинически очевидным.
Молекулярное профилирование, визуализация, аутоантитела и дерматоскопия могут использоваться для точной диагностики MUP (114, 115). В вышеупомянутом исследовании 32% респондентов также проверили образцы опухолей MUP на наличие мутаций BRAF, c-KIT и GNAQ, и наиболее распространенными методами визуализации были КТ и / или ПЭТ (109).Кроме того, аутоантитела к меластатину 1 (TRPM1) с временным рецепторным потенциалом могут быть полезны при разработке MUP (116). Dalal et al. описали пациента с двусторонним внутриглазным воспалением и кровоизлиянием в сетчатку относительно ретинопатии, связанной с меланомой, чье первоначальное обследование на меланому не выявило (116). Впоследствии у пациента были обнаружены положительные аутоантитела к TRPM1, что затем потребовало дополнительных изображений, которые выявили скрытую MUP с участием подмышечных лимфатических узлов (116). Наконец, различные группы предложили использовать дерматоскопию для систематического сужения области потенциальных возможных пигментных поражений для биопсии и для выявления слегка атипичных пигментных поражений с целью диагностики скрытой первичной меланомы (115, 117).
УПРАВЛЕНИЕ
Многочисленные серии случаев подтвердили консенсус о том, что пациенты с MUP должны получать раннее агрессивное хирургическое лечение так же, как пациенты MKP (6, 8, 100, 102, 118, 119). Совсем недавно когорта из 78 пациентов с MUP с LN или подкожным заболеванием, получавших региональную лимфаденэктомию или широкое местное иссечение, дополнительно поддерживает эти ранние рекомендации по лечению (120). Хотя частота местных рецидивов подкожного поражения после широкого местного иссечения с краями от одного до двух сантиметров была относительно высокой и составляла 65%, авторы пришли к выводу, что широкое местное иссечение по-прежнему остается лучшим вариантом лечения подкожного заболевания (120).Напротив, значительно более низкая частота местных рецидивов (11%) для поражения ЛУ после регионарной диссекции ЛУ подтверждает его использование в качестве стандарта лечения MUP с поражением ЛУ (120).
Более того, региональная лимфаденэктомия при пальпируемых метастазах в ЛУ была связана со значительным улучшением 5-летней общей выживаемости у пациентов с MUP стадии III по сравнению с пациентами MKP (39). Когда пациенты были подобраны на основе возраста, пола, бремени узловой опухоли и десятилетия постановки диагноза, средняя OS составила 164 месяца для пациентов с MUP по сравнению с 34 месяцами для пациентов с MKP (39).Подобные результаты были подтверждены в отдельной когорте пациентов с MUP, которые также продемонстрировали улучшенную выживаемость без болезней, отдаленных метастазов и выживаемость, специфичную для меланомы, для пациентов с MUP по сравнению с пациентами с MKP после терапевтического расслоения LN (121). Экстранодальное расширение, более трех положительных LN и адъювантная лучевая терапия были независимыми прогностическими факторами снижения безрецидивной и специфической для меланомы выживаемости у пациентов с MUP (121). Таким образом, отсутствие первичного участка не должно препятствовать агрессивному хирургическому вмешательству с регионарной лимфаденэктомией у пациентов III стадии MUP, и этих пациентов также следует рассматривать для адъювантной терапии, традиционно нацеленной на пациентов III стадии MKP (105, 122, 123).
Эти данные были подтверждены в систематическом обзоре MUP, проведенном Kamposioras et al. (3). Широкое местное иссечение или расслоение LN, радикальное или модифицированное, в сочетании с паротидэктомией, если необходимо, является текущим стандартом хирургического лечения MUP стадии III (3). Стадия IV MUP также требует агрессивной терапии, и ее следует лечить аналогично стадии IV MKP с комбинацией хирургического вмешательства, химиотерапии, иммунотерапии и лучевой терапии, поскольку медиана ОС и 5-летняя выживаемость для стадии IV MUP значительно выше, чем на стадии IV. MKP при сопоставлении с участком метастатического поражения (36).
ЗАКЛЮЧЕНИЕ
MUP, определяемый наличием меланомы в отдаленных подкожных участках, LN или висцеральных органах без очевидного первичного участка кожи, глаза или слизистой оболочки, является хорошо охарактеризованным в литературе объектом. Он составляет 3,2% всех новых диагнозов меланомы и чаще встречается у мужчин с пиком заболеваемости в четвертом и пятом десятилетиях жизни. Поражение ЛУ встречается чаще, чем подкожное или висцеральное заболевание, и чаще всего поражает подмышечные ЛУ.Кроме того, при MUP сообщалось о вовлечении большого количества висцеральных органов, и следует учитывать возможность первичных некожных меланом, возникающих в результате злокачественного перерождения эктопических меланоцитов, присутствующих во внутренних органах, включая желудочно-кишечный тракт.
MUP следует классифицировать как болезнь AJCC стадии III, если она диагностирована в LNs, или как заболевание подкожной клетчатки при первичном обращении, или как болезнь AJCC стадии IV, если она диагностируется во внутренних органах.Пациенты с MUP имеют лучшие прогнозы и улучшенную OS по сравнению с пациентами с MKP, соответствующими стадиям, что позволяет предположить, что иммунологически опосредованная регрессия первичного сайта может быть общим основным механизмом, объясняющим биологический феномен MUP. Учитывая улучшенную выживаемость, пациентам с MUP стадии III следует лечить с помощью широкого местного иссечения при подкожном заболевании и модифицированной или радикальной резекции LN при заболевании LN, и этим пациентам следует предложить участие в клинических испытаниях, а также аналогичную адъювантную терапию, как на стадии III Пациенты МКП.Наконец, пациентов с IV стадией MUP следует лечить агрессивно и аналогично пациентам с IV стадией MKP, сочетая хирургическое вмешательство, химиотерапию, иммунотерапию и лучевую терапию.
Благодарности: Эта работа была поддержана грантами Фонда семьи Чар и Чака Фаулеров и Фонда дерматологии.
Конфликт интересов: Авторы заявляют об отсутствии потенциального конфликта интересов в отношении исследования, авторства и / или публикации этой статьи.
Заявление об авторских правах и разрешении: Насколько нам известно, материалы, включенные в эту главу, не нарушают законы об авторских правах. Все первоисточники должным образом отмечены и / или указаны ссылки. В соответствующих случаях соответствующие разрешения были получены от первоначальных правообладателей.
ССЫЛКИ
- 1.
- Chang AE, Karnell LH, Menck HR. Национальная база данных по раку сообщает о кожной и некожной меланоме: сводка 84 836 случаев за последнее десятилетие.Комиссия по раку Американского колледжа хирургов и Американское онкологическое общество. Рак. 1998. 83 (8): 1664–78. [PubMed: 9781962] [CrossRef]
- 2.
- Дасгупта Т., Боуден Л., Берг Дж. У. Злокачественная меланома неизвестного первичного происхождения. Surg Gynecol Obstet. 1963; 117: 341–5. [PubMed: 14080349]
- 3.
- Kamposioras K, Pentheroudakis G, Pectasides D, Pavlidis N. Злокачественная меланома неизвестного первичного очага. Короче говоря. Систематический обзор литературы.Crit Rev Oncol Hematol. 2011. 78 (2): 112–26. [PubMed: 20570171] [CrossRef]
- 4.
- Bankar S, Patkar S, Desai S, Shrikhande SV. Необычное проявление меланомы неизвестного первичного происхождения: описание случая и обзор литературы. J Cancer Res Ther. 2015; 11 (4): 1025. [PubMed: 26881591] [CrossRef]
- 5.
- Smith JL Jr., Stehlin JS Jr. Спонтанная регрессия первичных злокачественных меланом с регионарными метастазами. Рак. 1965. 18 (11): 1399–415. [PubMed: 5844157] [CrossRef]
- 6.
- Панагопулос Э., Мюррей Д. Метастатическая злокачественная меланома неизвестного первичного происхождения: исследование 30 случаев. J Surg Oncol. 1983; 23 (1): 8–10. [PubMed: 6843134] [CrossRef]
- 7.
- Muchmore JH, Krementz ET, Carter RD, Sutherland CM, Mendoza EA. Изолированная перфузия конечностей при метастатической меланоме из неизвестного первичного очага. S Med J. 1986; 79 (3): 288–90. [PubMed: 3952537] [CrossRef]
- 8.
- Лопес Р., Холиок Э.Д., Мур Р.Х., Каракусис С.П. Злокачественная меланома с неизвестной первичной локализацией.J Surg Oncol. 1982; 19 (3): 151–4. [PubMed: 7070093] [CrossRef]
- 9.
- 10.
- Благословение К., Макларен К.М. Гистологический регресс первичной меланомы кожи: распознавание, распространенность и значение. Гистопатология. 1992. 20 (4): 315–22. [PubMed: 1577409] [CrossRef]
- 11.
- Анбари К.К., Шухтер Л.М., Баки Л.П., Мик Р., Синнестведт М., Герри Д.т. и др. Меланома неизвестной первичной локализации: представление, лечение и прогноз — исследование в одном учреждении.Группа изучения пигментных поражений Пенсильванского университета. Рак. 1997. 79 (9): 1816–21. [PubMed: 01] [CrossRef]
- 12.
- Джулиано А.Е., Мозли Х.С., Ирие РФ, Голуб Ш., Мортон Д.Л. Иммунологические аспекты неизвестной первичной меланомы. Операция. 1980. 87 (1): 101–5. [PubMed: 7350713]
- 13.
- Савойя П., Фава П., Оселла-Абате С., Нардо Т., Комессатти А., Куаглино П. и др. Меланома неизвестной первичной локализации: 33-летний опыт работы в Туринском центре меланомы. Melanoma Res. 2010. 20 (3): 227–32.[PubMed: 20449885] [CrossRef]
- 14.
- Clemente CG, Mihm MC Jr., Bufalino R, Zurrida S, Collini P, Cascinelli N. Прогностическое значение инфильтрирующих опухоль лимфоцитов в фазе вертикального роста первичной кожной меланомы. Рак. 1996. 77 (7): 1303–10. [PubMed: 8608507] [CrossRef]
- 15.
- Хаанен Дж. Б., Баарс А., Гомес Р., Ведер П., Смитс М., де Грюйл Т. Д. и др. Меланома-специфичные лимфоциты, инфильтрирующие опухоль, но не циркулирующие меланомо-специфические Т-клетки, могут предсказывать выживаемость у пациентов с удаленной меланомой на поздней стадии.Cancer Immunol Immunother. 2006; 55 (4): 451–8. [PubMed: 16034562] [CrossRef]
- 16.
- Салех Ф.Х., Кротти К.А., Херси П., Мензис С.В. Первичная регрессия опухоли меланомы, связанная с иммунным ответом на опухоль-ассоциированный антиген melan-A / MART-1. Int J Cancer. 2001. 94 (4): 551–7. [PubMed: 11745443] [CrossRef]
- 17.
- Hsueh EC, Gupta RK, Yee R, Leopoldo ZC, Qi K, Morton DL. Определяет ли эндогенный иммунный ответ исход хирургического лечения метастатической меланомы? Энн Сург Онкол.2000. 7 (3): 232–8. [PubMed: 10791855] [CrossRef]
- 18.
- Литвак Д.А., Гупта Р.К., Йи Р., Ванек Л.А., Йе В., Мортон Д.Л. Эндогенный иммунный ответ на меланому на ранней и промежуточной стадиях коррелирует с исходами и не зависит от локорегионального рецидива и стандартных прогностических факторов. J Am Coll Surg. 2004. 198 (1): 27–35. [PubMed: 14698308] [CrossRef]
- 19.
- Bodurtha AJ, Chee DO, Laucius JF, Mastrangelo MJ, Prehn RT. Клиническое и иммунологическое значение цитотоксических антител к меланоме человека.Cancer Res. 1975. 35 (1): 189–93. [PubMed: 1109788] [CrossRef]
- 20.
- Каневари С., Фоссати Г., Делла Порта Г., Бальзарини Г.П. Гуморальная цитотоксичность у больных меланомой и ее корреляция со степенью и течением заболевания. Int J Cancer. 1975. 16 (5): 722–9. [PubMed: 1184240] [CrossRef]
- 21.
- Льюис М.Г., Иконописов Р.Л., Нэрн Р.К., Филлипс TM, Фэрли Г.Х., Боденхэм округ Колумбия и др. Опухолевые антитела при злокачественной меланоме человека и их связь со степенью заболевания.Br Med J. 1969; 3 (5670): 547–52. [Бесплатная статья PMC: PMC1984348] [PubMed: 4896110] [CrossRef]
- 22.
- Morton DL, Malmgren RA, Holmes EC, Ketcham AS. Демонстрация антител против злокачественной меланомы человека методом иммунофлуоресценции. Операция. 1968; 64 (1): 233–40. [PubMed: 4173159]
- 23.
- 24.
- Шеной Б.В., Форт L 3-й, Бенджамин С.П. Первичная злокачественная меланома в лимфатическом узле. Дело о недостающем звене. Am J Surg Pathol. 1987. 11 (2): 140–6.[PubMed: 3812873] [CrossRef]
- 25.
- Sterchi JM, Muss HB, Weidner N. Клеточный синий невус, имитирующий метастатическую меланому: отчет о необычно большом поражении, связанном с агрегатами невус-клетки в регионарных лимфатических узлах. J Surg Oncol. 1987. 36 (1): 71–5. [PubMed: 3626565] [CrossRef]
- 26.
- Ридольфи Р.Л., Розен П.П., Талер Х. Клеточные агрегаты невуса, связанные с лимфатическими узлами: оценочная частота и клиническое значение. Рак. 1977; 39 (1): 164–71. [PubMed: 832230] [CrossRef]
- 27.
- Mancini L, Gubinelli M, Fortunato C, Carella R. Голубой невус капсулы лимфатического узла. Отчет о случае. Patologica. 1992. 84 (1092): 547–50. [PubMed: 1491897]
- 28.
- Манурас А., Генетзакис М., Лагудианакис Э., Маркогианнакис Х., Пападима А., Кафири Г. и др. Злокачественные меланомы желудочно-кишечного тракта неизвестного происхождения: следует ли считать их первичными? Мир Дж. Гастроэнтерол. 2007. 13 (29): 4027–9. [Бесплатная статья PMC: PMC4171183] [PubMed: 17663525] [CrossRef]
- 29.
- Дао А.Х., Пейдж Д.Л., Рейнольдс В.Х., Адкинс Р.Б. Младший. Первичная злокачественная меланома надпочечника. Отчет о двух случаях и обзор литературы. Am Surg. 1990. 56 (4): 199–203. [PubMed: 2194410]
- 30.
- Dutton-Regester K, Kakavand H, Aoude LG, Stark MS, Gartside MG, Johansson P, et al. Меланомы неизвестной первичной формы имеют мутационный профиль, соответствующий кожной меланоме, подвергшейся воздействию солнечных лучей. Pigment Cell Melanoma Res. 2013. 26 (6): 852–60. [PubMed: 238] [CrossRef]
- 31.
- Gos A, Jurkowska M, van Akkooi A, Robert C, Kosela-Paterczyk H, Koljenovic S, et al. Молекулярная характеристика узловых метастазов меланомы и неизвестного первичного очага и исходы у пациентов. Энн Сург Онкол. 2014. 21 (13): 4317–23. [Бесплатная статья PMC: PMC4218979] [PubMed: 24866436] [CrossRef]
- 32.
- Baiter M, Schuler G, Hartmann A, Schneider-Stock R, Heinzerling L. Патогенетические последствия распространения мутации BRAF у пациентов с меланомой стадии IV. Дерматология. 2015; 231 (2): 127–33.[PubMed: 26138035] [CrossRef]
- 33.
- Egberts F, Bergner I., Kruger S, Haag J, Behrens HM, Hauschild A, et al. Метастатическая меланома неизвестной первичной формы напоминает генотип меланомы кожи. Энн Онкол. 2014; 25 (1): 246–50. [PubMed: 24276025] [CrossRef]
- 34.
- 35.
- Egberts F, Kruger S, Behrens HM, Bergner I., Papaspyrou G, Werner JA, et al. Меланомы неизвестного первичного происхождения часто содержат мутации промотора TERT. Melanoma Res.2014. 24 (2): 131–6. [PubMed: 24463461] [CrossRef]
- 36.
- 37.
- Sutherland CM, Chmiel JS, Bieligk S, Henson DE, Winchester DP. Характеристики пациентов, лечение и исход неизвестной первичной меланомы в США в 1981 и 1987 гг. Am Surg. 1996. 62 (5): 400–6. [PubMed: 8615572]
- 38.
- Wang BY, Lawson W., Robinson RA, Perez-Ordonez B., Brandwein M. Злокачественные меланомы околоушной железы: сравнение выживаемости пациентов с метастазами из известных и неизвестных участков первичной опухоли.Arch Otolaryngol Head Neck Surg. 1999. 125 (6): 635–9. [PubMed: 10367919] [CrossRef]
- 39.
- Ли С.К., Фарис МБ, Ванек Л.А., Мортон Д.Л. Повышенная выживаемость после лимфаденэктомии по поводу узлового метастаза неизвестной первичной меланомы. J Clin Oncol. 2008. 26 (4): 535–41. [PubMed: 18235114] [CrossRef]
- 40.
- 41.
- Scott JF, Thompson CL, Vyas R, Honda K, Zender C, Rezaee R, et al. Меланома околоушной железы первичной неизвестной формы. J Cancer Res Clin Oncol.2016. 142 (7): 1529–37. [PubMed: 27075178] [CrossRef]
- 42.
- 43.
- Шеной А.С., Десаи Х.М., Кавишвар В.С., Савант Х.В. Метастатическая злокачественная меланома у молодого взрослого с неизвестной первичной. Индийский рак J. 2015; 52 (3): 446–7. [PubMed: 26
4] [CrossRef]
- 44.
- Пуджани М., Хассан М.Дж., Джетли С., Райна П.К., Кумар М. Злокачественная меланома, представленная как злокачественная меланома средостения, представляющая собой средостение неизвестного первичного происхождения? Turk Patoloji Derg.2017; 33 (2): 168–70. [PubMed: 25652557] [CrossRef]
- 45.
- Tanaka K, Tomita H, Hisamatsu K, Hatano Y, Yoshida K, Hara A. Острая печеночная недостаточность, связанная с диффузной инфильтрацией в печень злокачественной меланомы неизвестного первичного происхождения. Intern Med. 2015; 54 (11): 1361–4. [PubMed: 26027987] [CrossRef]
- 46.
- Танака М., Ватанабэ С., Масаки Т., Курокохчи К., Кинекава Ф., Иноуэ Х. и др. Фульминантная печеночная недостаточность, вызванная злокачественной меланомой неизвестного первичного происхождения.J Gastroenterol. 2004. 39 (8): 804–6. [PubMed: 15338379] [CrossRef]
- 47.
- Стагнитти Ф., Орсини С., Мартеллуччи А., Тудиско А., Аваллоне М., Айути Ф. и др. Инвагинация тонкой кишки из-за метастатической меланомы неизвестного первичного очага. История болезни. G Chir. 2014; 35 (9–10): 246–9. [Бесплатная статья PMC: PMC4321500] [PubMed: 25419593] [CrossRef]
- 48.
- Бланко Р., Родригес Вильяр Д., Фернандес-Пелло С., Балдиссера Дж. В., Диас Б., Вента В. и др. Массивная двусторонняя метастатическая меланома надпочечников оккультного происхождения: клинический случай.Анальный Кван Цитопатол Гистпатол. 2014; 36 (1): 51–4. [PubMed: 242]
- 49.
- Сузуки Т., Кусумото С., Иида С., Тада Т., Мори Ф. Амеланотическая злокачественная меланома неизвестного первичного происхождения с метастазами в костный мозг: отчет о клиническом случае и обзор литературы. Intern Med. 2014. 53 (4): 325–8. [PubMed: 24531089] [CrossRef]
- 50.
- 51.
- 52.
- 53.
- Хедаяти А.А., Бандурски Дж., Левандовски А.Бифокальный метастаз меланомы в тонкий кишечник из неизвестного первичного звена с кишечной непроходимостью — отчет о клиническом случае. Contemp Oncol (Познань). 2013. 17 (3): 317–20. [Бесплатная статья PMC: PMC3934062] [PubMed: 24596522] [CrossRef]
- 54.
- 55.
- Скарбез К., Фанчиулло Л. Метастатическая меланома неизвестного первичного происхождения, проявляющаяся как синдром дорсального среднего мозга. Optom Vis Sci. 2012; 89 (12): e112–17. [PubMed: 23142879] [CrossRef]
- 56.
- 57.
- Ениова О., Алтынбас А., Эрсой О., Айдынли М., Байрактар Ю. Метастатическая злокачественная меланома печени неизвестного происхождения. Turk J Gastroenterol. 2012. 23 (4): 420–1. [PubMed: 22965523] [CrossRef]
- 58.
- 59.
- 60.
- Mesa M, Quesada JL, Pinas J. Метастаз амеланотической меланомы неизвестного происхождения в околоушную железу. Br J Oral Maxillofac Surg. 2009. 47 (7): 569–71. [PubMed: 19167137] [CrossRef]
- 61.
- Wilkinson AR, Mahore SD, Bothale KA.Случай метастатической меланомы в груди с неизвестной первичной локализацией, диагностированной с помощью тонкоигольной аспирационной цитологии. Индийский J Pathol Microbiol. 2009. 52 (4): 587–8. [PubMed: 19805989] [CrossRef]
- 62.
- 63.
- де Уилт Дж. Х., Фармер С. Е., Скольер Р. А., МакКоган Британская Колумбия, Томпсон Дж. Ф. Изолированная меланома в легком, первичная локализация которой неизвестна: метастатическое заболевание или первичная опухоль легкого? Melanoma Res. 2005. 15 (6): 531–7. [PubMed: 16314739] [CrossRef]
- 64.
- Wagner MS, Shoup M, Pickleman J, Yong S. Первичная злокачественная меланома общего желчного протока: отчет о болезни и обзор литературы. Arch Pathol Lab Med. 2000. 124 (3): 419–22. [PubMed: 10705398]
- 65.
- Мерсер Н.С., Деварадж В.С. Внутримышечная метастатическая меланома с неизвестной первичной. Br J Plast Surg. 1990. 43 (3): 367–8. [PubMed: 2350647] [CrossRef]
- 66.
- Шеной С., Кассим Р. Метастатическая меланома в желудочно-кишечный тракт: роль хирургии как паллиативного лечения.W V Med J. 2013; 109 (1): 30–3. [PubMed: 23413546]
- 67.
- Коттеас Э.А., Адамопулос А., Дрогитис П.Д., Залонис А., Джаннопулос К.В., Карапанагиоту Э.М. и др. Желудочно-кишечное кровотечение как начальное проявление меланомы неизвестного первичного происхождения: отчет о случае и обзор литературы. In Vivo. 2009. 23 (3): 487–9. [PubMed: 19454519]
- 68.
- Shan GD, Xu GQ, Chen LH, Wang ZM, Jin EY, Hu FL, et al. Диффузная инфильтрация печени меланомой неизвестного первичного происхождения: отчет об одном случае и обзор литературы.Intern Med. 2009. 48 (24): 2093–6. [PubMed: 20009398] [CrossRef]
- 69.
- Basarici I, Demir I, Yilmaz H, Altekin RE. Обструктивная метастатическая злокачественная меланома сердца: неизбежная окклюзия легочной артерии, вызванная метастазами в правый желудочек с неизвестным происхождением первичной опухоли. Сердце легкое. 2006; 35 (5): 351–4. [PubMed: 16963367] [CrossRef]
- 70.
- 71.
- Менг М.В., Вербов Л.Х. Гематоспермия как симптом метастатической злокачественной меланомы неизвестного первичного происхождения.Урология. 2000; 56 (2): 330. [PubMed: 10925109] [CrossRef]
- 72.
- Levidou G, Korkolopoulou P, Papetta A, Patsouris E, Agapitos E. Лептоменингеальная меланома неизвестной первичной локализации: два случая с атипичным проявлением острого менингита. Clin Neuropathol. 2007. 26 (6): 299–305. [PubMed: 18232597] [CrossRef]
- 73.
- Примка Е.Дж. 3-й, Кинг С., О’Киф Е.Дж. Злокачественная меланома неизвестного происхождения, проявляющаяся как системный васкулит. Arch Dermatol. 1993. 129 (9): 1205–7.[PubMed: 8363413] [CrossRef]
- 74.
- Пальма Дж. А., Мартин-Альгарра С. Хроническая воспалительная демиелинизирующая полинейропатия, связанная с метастатической злокачественной меланомой неизвестного первичного происхождения. J Neurooncol. 2009. 94 (2): 279–81. [PubMed: 19266164] [CrossRef]
- 75.
- Kiratli H, Thirkill CE, Bilgic S, Eldem B, Kececi A. Паранеопластическая ретинопатия, связанная с метастатической кожной меланомой неизвестного первичного очага. Глаз (Лонд). 1997; 11: 889–92. Часть 6. [PubMed: 9537153] [CrossRef]
- 76.
- Manganoni AM, Farfaglia R, Sereni E, Farisoglio C, Pavoni L, Calzavara-Pinton PG. Меланома неизвестной первичной формы с узловыми метастазами, проявляющаяся депигментацией, напоминающей витилиго. G Ital Dermatol Venereol. 2012. 147 (2): 210–11. [PubMed: 22481586]
- 77.
- Sexton M, Snyder CR. Генерализованный меланоз при скрытой первичной меланоме. J Am Acad Dermatol. 1989. 20 (2): 261–6. Часть 1. [PubMed: 2915062] [CrossRef]
- 78.
- Занглис А., Стратаки А., Андреопулос Д., Сарафиану Э., Базиотис Н.Симметричная метастатическая меланома неизвестной первичной формы, проявляющаяся как синдром Горхэма-Стаута. Ад J Nucl Med. 2011. 14 (1): 78–80. [PubMed: 21512676]
- 79.
- 80.
- Ghosh SK, Bandyopadhyay D, Barma KD, Basu S, Roy A. Метастатическая меланома из неизвестного первичного очага, проявляющаяся в виде узелков цвета кожи и множественных висцеральных поражений. Кожаный. 2012; 10 (6): 396–9. [PubMed: 23346671]
- 81.
- Кумар М., ДеБоно Р., Соммерлад, Британская Колумбия. Метастатическая злокачественная меланома неизвестного первичного очага: случай возможного первичного проявления себя через 18 месяцев после вторичных.Br J Plast Surg. 1998. 51 (3): 258–9. [PubMed: 9664888] [CrossRef]
- 82.
- Eckert F, Baricevic B, Landthaler M, Schmid U. Метастатическая меланома из перстневидных клеток у пациента с неизвестной первичной опухолью. Гистологические, иммуногистохимические и ультраструктурные данные. J Am Acad Dermatol. 1992. 26 (5): 870–5. Часть 2. [PubMed: 1613153] [CrossRef]
- 83.
- Адлер MJ, Beckstead J, White CR Jr. Ангиоматоидная меланома: случай метастатической меланомы, имитирующей сосудистое злокачественное новообразование.Am J Dermatopathol. 1997. 19 (6): 606–9. [PubMed: 9415619] [CrossRef]
- 84.
- Schlagenhauff B, Stroebel W., Ellwanger U, Meier F, Zimmermann C, Breuninger H, et al. Метастатическая меланома неизвестного первичного происхождения имеет прогностическое сходство с региональной метастатической меланомой: Рекомендации для первичного обследования стадии. Рак. 1997. 80 (1): 60–5. [PubMed: 9210709] [CrossRef]
- 85.
- Хьюз М.С., Райт А., Барбур А., Томас Дж., Смитерс Б.М., Грин А.С. и др. Пациенты, перенесшие лимфаденэктомию по поводу меланомы III стадии известной или неизвестной первичной локализации, не различаются по исходам.Int J Cancer. 2013. 133 (12): 3000–7. [PubMed: 23754707] [CrossRef]
- 86.
- Rutkowski P, Nowecki ZI, Dziewirski W., Zdzienicki M, Pienkowski A, Salamacha M, et al. Меланома без детектируемого первичного очага с метастазами в лимфатические узлы. Dermatol Surg. 2010. 36 (6): 868–76. [PubMed: 20482725] [CrossRef]
- 87.
- Baab GH, McBride CM. Злокачественная меланома: пациент с неизвестным местом первичного происхождения. Arch Surg. 1975. 110 (8): 896–900. [PubMed: 1156155] [CrossRef]
- 88.
- Йонк А., Крун Б.Б., Рамке П., Муи В.Дж., Харт А.А., ван Донген Дж.А. Метастазы в лимфатические узлы от меланомы с неизвестным первичным локализацией. Br J Surg. 1990. 77 (6): 665–8. [PubMed: 2383736] [CrossRef]
- 89.
- 90.
- Оберхольцер PA, Urosevic M, Steinert HC, Dummer R. Базовая стадия меланомы с неизвестным первичным сайтом: значение сывороточного белка s100 и эмиссия позитронов томография. Дерматология. 2008. 217 (4): 351–5. [PubMed: 18799883] [CrossRef]
- 91.
- Pfeil AF, Leiter U, Buettner PG, Eigentler TK, Weide B, Meier F и др. Меланома неизвестной первичной формы правильно классифицирована по классификации меланомы AJCC от 2009 г. Melanoma Res. 2011. 21 (3): 228–34. [PubMed: 21502902] [CrossRef]
- 92.
- de Waal AC, Aben KK, van Rossum MM, Kiemeney LA. Меланома неизвестного первичного происхождения: популяционное исследование в Нидерландах. Eur J Cancer. 2013. 49 (3): 676–83. [PubMed: 23031553] [CrossRef]
- 93.
- Милтон GW, Шоу HM, McCarthy WH.Скрытая первичная злокачественная меланома: факторы, влияющие на выживаемость. Br J Surg. 1977. 64 (11): 805–8. [PubMed: 588977] [CrossRef]
- 94.
- Nasri S, Namazie A, Dulguerov P, Mickel R. Злокачественная меланома шейных и околоушных лимфатических узлов с неизвестной первичной локализацией. Ларингоскоп. 1994. 104 (10): 1194–8. [PubMed: 7934587] [CrossRef]
- 95.
- Кац К.А., Йонаш Э., Ходи Ф.С., Сойфер Р., Квиткивски К., Собер А.Дж. и др. Меланома неизвестного первичного происхождения: опыт работы в Массачусетской больнице общего профиля и в онкологическом институте Дана-Фарбер.Melanoma Res. 2005. 15 (1): 77–82. [PubMed: 15714125] [CrossRef]
- 96.
- Weide B, Faller C, Buttner P, Pflugfelder A, Leiter U, Eigentler TK, et al. Факторы прогноза пациентов с меланомой со сателлитными или транзитными метастазами на момент постановки диагноза III стадии. PLoS One. 2013; 8 (4): e63137. [Бесплатная статья PMC: PMC3639278] [PubMed: 23638183] [CrossRef]
- 97.
- Weide B, Faller C, Elsasser M, Buttner P, Pflugfelder A, Leiter U, et al. Пациенты с меланомой с неизвестной первичной локализацией или узловым рецидивом после первоначального диагноза имеют благоприятную выживаемость по сравнению с пациентами с синхронным метастазом в лимфатический узел и первичной опухолью.PLoS One. 2013; 8 (6): e66953. [Бесплатная статья PMC: PMC3692543] [PubMed: 23825594] [CrossRef]
- 98.
- Куаглино П., Маренко Ф., Оселла-Абате С., Каппелло Н., Ортончелли М., Саломоне Б. и др. Витилиго является независимым благоприятным прогностическим фактором у пациентов с метастатической меланомой III и IV стадий: результаты наблюдательного когортного исследования в одном учреждении на базе стационара. Энн Онкол. 2010. 21 (2): 409–14. [PubMed: 19622589] [CrossRef]
- 99.
- Духра П., Ильчишин А. Длительная выживаемость при метастатической злокачественной меланоме, связанной с витилиго.Clin Exp Dermatol. 1991. 16 (4): 303–5. [PubMed: 1794178] [CrossRef]
- 100.
- Рейнтген Д.С., Маккарти К.С., Вудард Б., Кокс Е., Зиглер Х.Ф. Метастатическая злокачественная меланома неизвестного происхождения. Surg Gynecol Obstet. 1983. 156 (3): 335–40. [PubMed: 6828979]
- 101.
- Велес А., Уолш Д., Каракусис С.П. Лечение первичной меланомы неизвестного происхождения. Рак. 1991. 68 (12): 2579–81. [PubMed: 1933805] [CrossRef]
- 102.
- Чанг П., Кнаппер WH. Метастатическая меланома неизвестной первичной формы.Рак. 1982. 49 (6): 1106–11. [PubMed: 7059936] [CrossRef]
- 103.
- Сантини Х., Байерс Р.М., Вольф П.Ф. Метастатическая меланома в шейные и околоушные узлы из неизвестного первичного местоположения. Am J Surg. 1985. 150 (4): 510–12. [PubMed: 4051118] [CrossRef]
- 104.
- Vijuk G, Coates AS. Выживаемость пациентов с висцеральной метастатической меланомой из скрытого первичного поражения: ретроспективное когортное исследование. Энн Онкол. 1998. 9 (4): 419–22. [PubMed: 9636833] [CrossRef]
- 105.
- Prens SP, van der Ploeg AP, van Akkooi AC, van Montfort CA, van Geel AN, de Wilt JH, et al. Результат терапевтического рассечения лимфатических узлов у пациентов с неизвестным локализацией первичной меланомы. Энн Сург Онкол. 2011; 18 (13): 3586–92. [Бесплатная статья PMC: PMC3222814] [PubMed: 21611857] [CrossRef]
- 106.
- Кук Д., Шуштари А.Н., Баркер К.А., Панагеас К.С., Мунхоз Р.Р., Момтаз П.и др. Прогноз слизистой, увеальной, акральной, некакральной кожной и неизвестной первичной меланомы с момента первого метастазирования.Онколог. 2016; 21 (7): 848–54. [Бесплатная статья PMC: PMC4943393] [PubMed: 27286787] [CrossRef]
- 107.
- Bae JM, Choi YY, Kim DS, Lee JH, Jang HS, Lee JH, et al. Метастатические меланомы неизвестных первичных имеют лучший прогноз, чем таковые при известных первичных: систематический обзор и метаанализ обсервационных исследований. J Am Acad Dermatol. 2015; 72 (1): 59–70. [PubMed: 25440435] [CrossRef]
- 108.
- Tos T, Klyver H, Drzewiecki KT. Обширный скрининг первичной опухоли является избыточным при меланоме неизвестной первичной опухоли.J Surg Oncol. 2011. 104 (7): 724–7. [PubMed: 21721009] [CrossRef]
- 109.
- 110.
- Галли Ф., Петрайтиене В., Муту С.К., Джеймс С., Коппана В.Р., Арья А. Проблемы дифференциальной диагностики саркомы межпальцевых дендритных клеток при интрапаротиде лимфатический узел против метастатической злокачественной меланомы с неизвестной первичной локализацией. Int J Surg Pathol. 2015; 23 (3): 248–52. [PubMed: 25722315] [CrossRef]
- 111.
- Biernacka A, Linos KD, DeLong PA, Suriawinata AA, Padmanabhan V, Liu X.Случай меланомы с отрицательным результатом S-100: диагностическая ловушка при обследовании низкодифференцированной метастатической опухоли неизвестного происхождения. Цитожурнал. 2016; 13:21. [Бесплатная статья PMC: PMC5040106] [PubMed: 27729935] [CrossRef]
- 112.
- Azoury SC, Crompton JG, Straughan DM, Klemen ND, Reardon ES, Beresnev TH, et al. Неизвестная первичная меланома носоглотки, проявляющаяся тяжелым рецидивирующим носовым кровотечением и потерей слуха после лечения и ремиссии метастатического заболевания: отчет о клиническом случае и обзор литературы.Int J Surg Case Rep. 2015; 10: 232–5. [Бесплатная статья PMC: PMC4430121] [PubMed: 25898283] [CrossRef]
- 113.
- Sciacca V, Ciorra AA, Di Fonzo C, Rossi R, Pistillucci G, Lugini A, et al. Долгосрочная выживаемость метастатической меланомы в подвздошную кишку с признаками первичного кожного заболевания после 15 лет наблюдения: отчет о клиническом случае. Тумори. 2010. 96 (4): 640–3. [PubMed: 20968150]
- 114.
- 115.
- de Giorgi V, Stante M, Carli P. Неизвестная первичная меланома.Eur J Cancer. 2004. 40 (9): 1454–145. [PubMed: 15177507] [CrossRef]
- 116.
- Dalal MD, Morgans CW, Duvoisin RM, Gamboa EA, Jeffrey BG, Garg SJ, et al. Диагностика скрытой меланомы с использованием тестирования аутоантител меластатина 1 (TRPM1) с временным рецепторным потенциалом: новый подход. Офтальмология. 2013; 120 (12): 2560–4. [Бесплатная статья PMC: PMC4928578] [PubMed: 24053997] [CrossRef]
- 117.
- Stante M, de Giorgi V, Carli P. Возможная роль дерматоскопии в обнаружении первичной кожной меланомы неизвестного происхождения.J Eur Acad Dermatol Venereol. 2006. 20 (3): 299–302. [PubMed: 16503891] [CrossRef]
- 118.
- Клауснер Дж. М., Гутман М., Инбар М., Розин Р. Р.. Неизвестная первичная меланома. J Surg Oncol. 1983. 24 (2): 129–31. [PubMed: 6632893] [CrossRef]
- 119.
- 120.
- 121.
- van der Ploeg AP, Haydu LE, Spillane AJ, Scolyer RA, Quinn MJ, Saw RP и др. Пациенты с меланомой с неизвестным локализацией первичной опухоли имеют лучший результат, чем пациенты с известной первичной опухолью, после терапевтической диссекции лимфатических узлов при макроскопическом (клинически пальпируемом) поражении лимфоузлов.Энн Сург Онкол. 2014. 21 (9): 3108–16. [PubMed: 24802907] [CrossRef]
- 122.
- О’Нил Дж., Хундар Р., Ноулз Л., Скотт-Янг Н., Орландо А. Меланома с неизвестным первичным заболеванием — серия случаев. J Plast Reconstr Aesthet Surg. 2010. 63 (12): 2071–80. [PubMed: 20335085] [CrossRef]
- 123.
- Келли Дж., Редмонд HP. Меланома неизвестного происхождения: серия случаев. Ir J Med Sci. 2010. 179 (4): 629–32. [PubMed: 19639362] [CrossRef]
Меланома Американская ассоциация кожи
ЗАЩИТА ОТ СОЛНЦА — самый простой и эффективный способ снизить риск рака кожи.Держитесь подальше от солнца, когда солнце наиболее сильное (с 10:00 до 16:00). Наносите достаточное количество солнцезащитного крема широкого спектра действия (с защитой от UVA / UVB и SPF 30+) круглый год на все открытые участки кожи. Выходя на улицу, надевайте защитную одежду, например головные уборы и солнцезащитные очки.
Что такое меланома?
Меланома — опасная для жизни злокачественная опухоль, которая возникает в клетках, называемых меланоцитами, которые являются клетками, вырабатывающими пигмент. Большинство меланом бывает черного или коричневого цвета. Однако некоторые меланомы имеют цвет кожи, розовый, красный, фиолетовый, синий или белый цвет.
Меланома начинается на коже, где ее легко увидеть и вылечить. Однако он может врастать в кожу, достигая кровеносных сосудов и лимфатических сосудов, а также может распространяться по телу на различные органы, когда это может быть фатальным. Если его распознать и лечить на ранней стадии, шансы на выздоровление очень высоки. Но если его не обнаружить на ранней стадии, он может глубже проникнуть в кожу и распространиться на другие части тела. Как только меланома распространяется за пределы кожи на другие части тела, ее становится трудно лечить и она может привести к летальному исходу.
Заболеваемость меланомой растет во всем мире. Средний возраст постановки диагноза — 59 лет, а средний возраст смерти от меланомы — 67 лет.
Кто подвержен риску развития меланомы?
Каждый человек подвержен определенному риску развития меланомы, но повышенный риск зависит от нескольких факторов. Это воздействие солнца, количество родинок на коже, тип кожи и семейный анамнез (генетика).
- Воздействие на солнце — Лучи UVA и UVB опасны для кожи и могут вызвать рак кожи, включая меланому.Солнечные ожоги с волдырями в раннем детстве увеличивают риск, но кумулятивное воздействие также является фактором.
- Родинки — Люди с множеством родинок подвергаются повышенному риску развития меланомы. Люди с более чем 50 родинками подвергаются большему риску. У некоторых людей есть родинки неправильной формы и необычного вида, которые называются атипичными или диспластическими невусами. Это увеличивает риск меланомы.
- Семейный анамнез — Любой человек, у кого-либо из родственников первой степени (мать, отец, братья, сестры или дети) с диагнозом меланома, имеет на пятьдесят процентов больше шансов заболеть меланомой, чем человек, не имеющий семейной истории меланомы.
- Генетический риск — Мутация в гене BRAF, может играть определенную роль в возникновении меланомы. Мутации в этом гене могут привести к неконтролируемому росту клеток и раку. Мутации, наиболее часто встречающиеся при семейной меланоме, происходят в другом гене, которым является р53.
- Личный анамнез — Человек, у которого в анамнезе был другой тип рака кожи, такой как базальноклеточная карцинома или плоскоклеточный рак, имеет повышенный риск развития меланомы.
- Тип кожи — Более светлая кожа подвержена повышенному риску развития меланомы.
- Иммунная система — Любой человек с ослабленной иммунной системой имеет повышенный шанс развития меланомы. Иммунная система может быть нарушена в результате химиотерапии, ВИЧ / СПИДа или трансплантации органов.
Как диагностируется меланома?
Родинки, также называемые невусами, представляют собой группы нормально выглядящих клеток меланоцитарного происхождения в дерме. Это безвредные коричневые пятна на коже. Меланома обычно отличается от обычных родинок. Лучший способ найти подозрительные родинки на теле — пройти обследование кожи на предмет наличия ABCDE меланомы.Первым признаком меланомы часто бывает изменение размера, формы или цвета родинки.
Меланома также может выглядеть как новая, черная, ненормальная или «некрасивая» родинка. В редких случаях меланома не имеет пигментации и ее сложнее диагностировать. Это также может выглядеть как незаживающая язва или новый шрам на коже.
Контрольный список меланомы:
Осмотрите себя с головы до пят и проверьте, нет ли следующих изменений в родинке.
Если вы увидите одно или несколько, немедленно обратитесь к дерматологу.
Какие бывают типы меланомы?
Меланомы делятся на четыре основные категории.
- Меланома с поверхностным распространением — Это наиболее распространенный тип, на который приходится около 70 процентов всех случаев. Часто наблюдается у молодых людей. При этом типе меланома довольно долго проходит по верхнему слою кожи, прежде чем проникнуть глубже.
- Lentigo Maligna — Этот тип меланомы чаще всего встречается у пожилых людей, возникая на постоянно подвергающейся воздействию солнечного света поврежденной коже лица, ушей, рук и верхней части туловища.
- Акральная лентигинозная меланома — Обычно проявляется в виде черного или коричневого обесцвечивания под ногтями, на подошвах стоп или ладонях рук. Он распространяется поверхностно, прежде чем проникнуть глубже. Это наиболее распространенная меланома у афроамериканцев и азиатов и наименее распространенная среди кавказцев.
- Узловая меланома — Обычно это инвазивное заболевание на момент постановки первого диагноза. Обычно он черный, но иногда бывает синим, серым, белым, коричневым, коричневым, красным или телесным оттенком.
Как определяется стадия меланомы?
Меланома делится на 4 стадии в зависимости от глубины первичной опухоли и того, насколько далеко рак распространился от начальной точки. Система определения стадии меланомы помогает определить лучший метод лечения для отдельных случаев, а также помогает определить прогноз. У меланомы in situ отличный прогноз после хирургического иссечения с достаточным хирургическим запасом. Инвазивные меланомы гораздо серьезнее. Толщина Бреслоу — это глубина меланомы, рассчитанная перпендикулярно поверхности кожи, в частности, от гранулезного слоя эпидермиса до самого нижнего уровня меланомы (в мм).
Какие методы лечения доступны?
Раннее выявление — лучшее лечение, поскольку оно значительно увеличивает шансы на выживание. Любое подозрительное поражение должно быть немедленно осмотрено дерматологом, который затем подтвердит диагноз, сделав биопсию кожи и определив наличие раковых клеток под микроскопом. Осмотр поражения под увеличением с помощью дерматоскопа перед выполнением биопсии улучшил клинический диагноз меланоцитарного поражения, но не заменил гистопатологический диагноз.Если обнаружена меланома, следующим первым шагом обычно является хирургическое иссечение всего поражения с окружающим его краем нормальной ткани.
- Хирургическое иссечение
Хирургическое удаление — это первый шаг в лечении всех стадий меланомы. Исходя из патологических особенностей опухоль, ее удаляют полностью вместе с окружающей нормальной тканью. Эта процедура снижает вероятность того, что раковые клетки останутся позади. Поля для иссечения определяется инвазией опухоли.Эта процедура проводится под местной анестезией дерматологом или хирургом в амбулаторных условиях.
При инвазивной меланоме может потребоваться биопсия сторожевого лимфатического узла. Биопсия сторожевого лимфатического узла — это процедура, при которой рядом с меланомой вводится радиоактивное вещество. Первый лимфатический узел (узлы), принимающий вещество, называется сигнальным лимфатическим узлом (узлами). (Это визуализирующее исследование называется лимфосцинтиграфией). Хирург удаляет сторожевые узлы, чтобы проверить наличие раковых клеток.
Если меланома распространилась на близлежащие лимфатические узлы (сторожевые лимфатические узлы), пораженные лимфатические узлы удаляются хирургическим путем. Эта процедура называется лимфодиссекцией, при которой хирург удаляет все лимфатические узлы в области меланомы.
- Адъювантное лечение
Обычно полное хирургическое удаление меланомы — единственное лечение, необходимое для людей с меланомой на ранней стадии (более тонкие меланомы, не распространившиеся на лимфатические узлы) при регулярных последующих посещениях дерматолога.
На поздних стадиях меланомы (толстые меланомы или меланомы, распространившиеся на близлежащие лимфатические узлы) могут потребоваться другие методы лечения, помимо хирургического вмешательства. Это называется «адъювантным» лечением и может принимать форму:
- Химиотерапия — В ней используются вещества, аналогичные тем, которые вырабатывает иммунная система организма, для уничтожения раковых клеток. Два типа иммунотерапии, используемые при меланоме, — это интерферон альфа и интерлейкин-2, которые можно назначать после операции пациентам с метастатической меланомой или высоким риском рецидива.
- Химиотерапия — Использует лекарства для уничтожения раковых клеток. Обычно это проводится циклами, при которых за периодом лечения следует период восстановления. Некоторые химиотерапевтические агенты обладают умеренной активностью при меланоме. DTIC (дакарбазин) является единственным наиболее активным агентом при меланоме с частотой ответа 15-20%. Подкожные поражения, лимфатические узлы и легочные поражения, скорее всего, будут реагировать на DTIC. Другие препараты, особенно цисплатин и кармустин, также обладают значительной активностью против меланомы.
- Лучевая терапия — Использует лучи высокой энергии для уничтожения раковых клеток. Это помогает уменьшить опухоль и облегчает симптомы. Он используется при запущенном заболевании (стадия IV), которое распространилось на мозг, кости или другие органы.
Меланома, распространившаяся на отдаленные участки тела, такие как легкие или печень, не поддается лечению. В этих случаях лечение обычно направлено на облегчение симптомов и обеспечение максимального комфорта для людей.
Люди с запущенной меланомой могут быть включены в клинические испытания, чтобы опробовать новое и экспериментальное лечение, такое как интерлейкины, фактор некроза опухоли, генная терапия, вакцины против меланомы.
Как предотвратить меланому?
- Уменьшение воздействия солнца — Лучший способ предотвратить меланому — сократить время пребывания на солнце. Избегайте солнца с 10 до 16 часов.
- Носите солнцезащитную и защитную одежду. — Нанесите обильное количество солнцезащитного крема на все открытые участки тела, нанесите за 20–30 минут до выхода на солнце и повторно нанесите каждые два часа. Используйте солнцезащитный крем широкого спектра действия с фактором защиты не менее 15.Носите защитную одежду, включая длинные рукава, длинные брюки, шляпы с широкими полями и солнцезащитные очки.
- Самостоятельный осмотр кожи — Каждые 6-8 недель следует проводить с головы до ног, чтобы найти подозрительные родинки. Важно всегда проверять свою кожу на предмет изменений в родинках (ABCDE) или появления новых родинок.
Чтобы узнать больше о меланоме и клинических испытаниях, посетите следующие веб-сайты:
Сорокалетний прогноз после брахитерапии увеальной меланомы
Описательная статистика
Для анализа подходили 677 пациентов с 677 увеальной меланомой, происходящей из сосудистой оболочки или цилиарного тела.Их средний возраст на момент постановки диагноза составлял 62 года (стандартное отклонение (SD) 14) с аналогичным соотношением мужчин (46%) и женщин (54%), а также правого (47%) и левого (53%) глаза. Средняя толщина на вершине опухоли составляла 5,2 мм (стандартное отклонение 2,5), а средний диаметр — 10,1 мм (стандартное отклонение 3,8). 659 из 677 опухолей (97%) относились к Т-категории 1, 2 или 3 согласно классификации Американского объединенного комитета по раку (AJCC). Средняя доза облучения составила 93,9 Гр (Гр) на верхушке опухоли (SD 18,5) и 633,6 Гр на поверхности склеры (SD 371.6). Медиана наблюдения составила 25,4 года (стандартное отклонение 5,2, таблица 1).
Таблица 1 Характеристики пациентов и опухолей, включенных в это исследование.Выживаемость
Из 677 включенных пациентов 533 (79%) скончались до окончания периода наблюдения. Из этих 533 пациентов 209 (39%) умерли от увеальной меланомы. Смертность, связанная с увеальной меланомой, составила 18% через 5 лет после брахитерапии бляшками, 28% через 10 лет, 32% через 15 лет, 35% через 20 лет и 36% через 25, 30, 35 и 40 лет, согласно кумулятивному анализу заболеваемости. .(Таблица 2). Из 209 смертей, связанных с увеальной меланомой, 119 (57%) произошли в течение 5 лет после брахитерапии бляшек. 172 (82%) произошли в течение первого десятилетия, а 195 из 209 (93%) — в течение 15 лет. Только 3 смертельных случая, связанных с увеальной меланомой, произошли у 212 пациентов, выживших более 20 лет после брахитерапии, и не было случаев смерти, связанных с увеальной меланомой, у 124 пациентов, живущих более 25 лет. Смертность от всех причин составила 27% в 5 лет, 45% в 10 лет, 57% в 15 лет, 69% в 20 лет, 77% в 25 лет, 81% в 30 лет, 84% в 35 лет и 86% в 40 лет (таблица 2).
Таблица 2 Кумулятивная смертность от увеальной меланомы и от всех причин.Каплан – Мейер
Выживаемость при конкретном заболевании не соответствовала медиане. Средняя выживаемость при конкретном заболевании составила 27,8 года (95% доверительный интервал (ДИ) 26,5–29,1, рис. 1). Выживаемость, специфичная для болезни Каплана-Мейера, составила 98% через 1 год, 82% через 5 лет, 72% через 10 лет, 68% через 15 лет, 65% через 20 лет и 64% через 25-40 лет. Медиана общей выживаемости составила 12,3 года (95% ДИ 10,7–13,9, рис. 2).
Рис. 1Кривая Каплана – Мейера, кумулятивная доля выживаемости, характерной для конкретного заболевания, после брахитерапии увеальной меланомы.
Рис. 2Кривая Каплана – Мейера, кумулятивная общая доля выживаемости после брахитерапии увеальной меланомы.
Относительная выживаемость
Наблюдаемая выживаемость пациентов с увеальной меланомой составила 97% через 1 год после брахитерапии бляшек. 73% через 5 лет после брахитерапии, 55% через 10 лет, 43% через 15 лет, 31% через 20 лет, 23% через 25 лет, 19% через 30 лет, 16% через 35 лет и 14% через 40 лет . Ожидаемая доля выживаемости людей того же пола и возраста в том же календарном году, что и наши пациенты, составляла 100% через 1 год после брахитерапии, 99% через 5 лет, 86% через 10 лет, 67% через 15 лет. лет, 50% в 20 лет, 33% в 25 лет, 23% в 30 лет, 14% в 35 лет и 7% в 40 лет (рис.3а). Следовательно, относительная выживаемость составила 97% через 1 год, 74% через 5 лет, 64% через 10 лет, 64% через 15 лет, 62% через 20 лет, 70% через 25 лет, 83% через 30 лет, 114 % в 35 лет и 200% в 40 лет (рис. 3b, таблица 3).
Рис. 3(a) Совокупная наблюдаемая (синий) и ожидаемая (красный) пропорции выживаемости после брахитерапии увеальной меланомы. (b) Совокупная относительная выживаемость после брахитерапии увеальной меланомы (синяя линия).Зеленые линии представляют пределы 95% доверительного интервала.
Таблица 3 Суммарная наблюдаемая, ожидаемая и относительная выживаемость.Выжившие в течение длительного периода времени
209 из наших 677 пациентов, умерших от своей болезни, на момент постановки диагноза были того же возраста, что и 468 пациентов, которые выжили или умерли от других причин (62 года по сравнению с 61 годом, t-тест Стьюдента p = 0,468) и имели опухоли на таком же расстоянии от диска зрительного нерва ( p = 0,494), но у них были опухоли значительно большего размера (диаметр p <0.001, толщина p <0,001, AJCC T-категория p <0,001) на значительно более продвинутой анатомической стадии (стадия AJCC p <0,001).
Из первоначально 677 пациентов 373 (55%) выжили 10 лет или дольше после брахитерапии бляшек. Эти пациенты были значительно моложе на момент постановки диагноза (t-критерий Стьюдента p <0,001) и имели опухоли значительно меньшего диаметра ( p <0,001), более тонкую апикальную толщину ( p <0.001) и более низкую стадию AJCC ( p <0,001), чем у пациентов, умерших в течение 10 лет. Однако расстояние от опухоли до диска зрительного нерва существенно не различалось между группами ( p = 0,566, таблица 4a).
Таблица 4 Средние характеристики пациента и опухоли для пациентов, живущих короче и дольше, чем (а) 10 лет, (б) 20 лет, (в) средние характеристики пациента и опухоли для пациентов с более коротким и более длительным периодом наблюдения — вверх.212 пациентов (31%) прожили 20 лет и более.Точно так же они были значительно моложе на момент постановки диагноза ( p <0,001) и имели опухоли значительно меньшего диаметра ( p <0,001), более тонкую апикальную толщину ( p = 0,033) и более низкую стадию AJCC ( p <0,001). ). Расстояние от опухоли до диска зрительного нерва существенно не различалось между группами ( p = 0,131, таблица 4b).
54 пациента (8%) имели период наблюдения 30 лет или дольше. Остальные 623 были либо мертвы, либо сроки наблюдения были короче.В отличие от групп выживших через 10 и 20 лет, единственными значимыми различиями для этих пациентов были возраст на момент постановки диагноза ( p <0,001) и диаметр опухоли ( p <0,019). Апикальная толщина опухоли, стадия AJCC и расстояние до диска зрительного нерва существенно не отличались от пациентов с более коротким периодом наблюдения (таблица 4c).
В бинарной логистической регрессии: возраст пациента на момент постановки диагноза, диаметр опухоли, толщина опухоли, стадия AJCC, расстояние до диска зрительного нерва и местный рецидив в качестве ковариант, возраст пациента на момент постановки диагноза (отношение шансов 0.96 за год увеличения, p <0,001) и диаметр опухоли (отношение шансов 0,84 на увеличенный мм, p = 0,004), но никакие другие переменные не были независимыми предикторами выживаемости через 10 лет или дольше после брахитерапии бляшек. Точно так же возраст пациента на момент постановки диагноза (отношение шансов 0,92 на увеличенный год, p <0,001) и диаметр опухоли (отношение шансов 0,86 на увеличенный мм, p = 0,017) были независимыми предикторами выживаемости 20 лет или дольше. Только возраст пациента на момент постановки диагноза (отношение шансов 0.91 за год увеличения, p <0,001) был независимым предиктором выживаемости через 30 или более лет после брахитерапии бляшек.
регрессия Кокса
Риск регрессии Кокса для смертности, связанной с увеальной меланомой, составил 0,21 через 5 лет, 0,32 через 10 лет, 0,39 через 15 лет и 0,44 через 20 лет (рис. 4). В многофакторном анализе с учетом возраста пациента на момент постановки диагноза, диаметра опухоли, толщины опухоли, стадии AJCC, расстояния до диска зрительного нерва и местного рецидива в качестве ковариант, диаметр опухоли (отношение рисков 1.1 на увеличенный мм, 95% ДИ 1,0–1,3, p = 0,006) и местный рецидив (отношение рисков 1,1, 95% ДИ 1,1–2,4, p = 0,015) были независимыми предикторами смертности, связанной с увеальной меланомой ( Таблица 5).
Рисунок 4Кумулятивный риск регрессии Кокса для смертности от меланомы (0,21 через 5 лет, 0,32 через 10 лет, 0,39 через 15 лет и 0,44 через 20 лет).
Таблица 5 Многомерный анализ пропорциональных рисков Кокса.Меланома у собак | Расположение, симптомы и варианты лечения
Резюме
Меланома — это рак, который возникает в результате нерегулируемой пролиферации меланоцитов, клеток, несущих пигмент, которые находятся в коже и слизистых оболочках млекопитающих.Пожилые собаки особенно предрасположены к этому раку, особенно к его очень агрессивной оральной форме. Фактически, меланома ротовой полости составляет почти 40% всех опухолей полости рта у собак.
Меланома у кошек считается редкостью, но, тем не менее, может поражать кожу или глаза.
Опухоли меланомы могут вести себя по-разному. Некоторые из них чрезвычайно агрессивны не только потому, что они могут быть сильно инвазивными, но также потому, что они имеют тенденцию легко распространяться в отдаленные ткани (метастазы).Хотя трудно предсказать, местоположение опухоли, толщина или глубина первичной опухоли, а также свойства самих раковых клеток используются для прогнозирования поведения опухолей меланомы.
Хотя меланомы кожи обычно доброкачественные и легко поддаются лечению, очень агрессивные злокачественные меланомы могут возникать где угодно на коже. Однако чаще глаза, подушечки ног, ногтевые ложа и места, где кожа встречается со слизистыми оболочками (например, на губе), являются местами, где, как правило, возникают агрессивные опухоли.Как и в случае опухолей полости рта, они могут быть местно инвазивными и быстро метастазировать в местные лимфатические узлы и, в конечном итоге, в отдаленные органы, такие как легкие и печень.
К сожалению, прогноз для большинства пациентов со злокачественной меланомой плохой, если не будет выбрано агрессивное лечение. В случае меланомы собак предполагается некоторая генетическая предрасположенность. В отличие от человеческой формы ультрафиолетовый свет не считается фактором развития этого заболевания у собак.
Симптомы и идентификация
Проявление меланомы зависит от пораженного участка: в случае меланомы полости рта владельцы обычно первыми замечают такие симптомы, как неприятный запах изо рта и неправильное жевательное поведение.Поскольку эти опухоли могут поражать подлежащую кость, в конечном итоге часто наблюдаются деформация, боль, кровотечение и потеря зубов. Также могут стать очевидными кровотечение изо рта, плохой аппетит или потеря веса.
В других местах, таких как подушечки стопы или пальцы ног, владельцы могут заметить боль, кровотечение или хромоту, если не само образование. Опухоль черного цвета наиболее типична для меланомы; однако все 17% меланом являются непигментированными («амеланотическими») и не будут иметь характерный черный цвет.
При диагностике меланомы настоятельно рекомендуются следующие тесты:
Физикальное обследование
Общий анализ крови
Панель биохимии крови
Анализ мочи
Грудная клетка X- лучей
Тонкоигольный аспират местных лимфатических узлов
УЗИ брюшной полости
Тонкоигольный аспират опухоли
Биопсия опухоли
Как и многие другие виды рака, болезнь может только поставить точный диагноз путем извлечения образца из пораженных тканей (биопсия) и его оценки с помощью гистопатологии (микроскопический анализ тканей сертифицированным патологом).Это может потребовать или не потребовать анестезии или седативных средств.
Гистопатологическая оценка опухоли важна для прогнозирования поведения рака. Патологоанатомы сделают ряд определений, которые помогут направить лечение.
Если необходимо рассмотреть возможность лечения, также необходимы рентген грудной клетки и тонкоигольная аспирация близлежащих лимфатических узлов. Также может быть рекомендовано УЗИ брюшной полости. Эти тесты помогают определить степень прогрессирования заболевания и составить индивидуальный план лечения пациента.
Поскольку трудно полностью оценить размер краев опухоли полости рта, КТ обычно рекомендуется перед операцией или облучением новообразования меланомы полости рта. Это помогает определить границы хирургического вмешательства хирурга и целевую зону онколога-радиолога, соответственно.
Также может быть проведен анализ костного мозга для определения стадии развития болезни и оказания помощи в лечении.
Затронутые породы
Сообщалось, что меланома полости рта поражает более мелкие породы, такие как кокер-спаниели и миниатюрные пудели, но одно исследование показало, что меланома или сам язык, по-видимому, преимущественно поражают более крупных собак — чау-чау и другие породы с сильной пигментацией языка, в частности.Следующие породы считаются предрасположенными ко всем формам меланомы:
У кошек генетической предрасположенности не выявлено.
Лечение
Меланома обычно лечится хирургическим путем. Хотя опухоли кожи, ногтевого ложа и подушечек ног часто иссекают врачи общей практики, меланома полости рта обычно считается областью сертифицированного хирурга. Какими бы инвазивными они ни были, чистые поля обычно достигаются только с помощью агрессивных узкоспециализированных хирургических методов.
Тем не менее, собакам с агрессивными меланомами не следует полагаться только на хирургическое лечение. Скорость метастазирования слишком высока. Фактически, собаки, подвергшиеся хирургическому лечению очень маленьких опухолей ротовой полости (без каких-либо признаков отдаленного распространения во время операции), живут всего около 17 месяцев. Но если эти опухоли были более 2 см в диаметре, собаки жили только 5,5 месяцев после операции.
Эти пугающие статистические данные объясняют, почему лечение меланомы часто предполагает также использование системных химиотерапевтических препаратов.Хотя исторически она менее эффективна, чем химиотерапия в случае других видов рака (например, лимфомы), тем не менее, она рекомендуется в качестве средства, помогающего отсрочить метастазирование.
Лучевая терапия — еще один распространенный метод лечения меланом, особенно когда чистые края невозможно получить хирургической резекцией. Фактически, сейчас радиация иногда полностью заменяет хирургическую резекцию. Однако вероятность успеха этого подхода в значительной степени зависит от местоположения меланомы.
Самая многообещающая терапия меланомы связана с недавней разработкой вакцины, специально нацеленной на ее аномальные опухолевые клетки. Вакцина делает это, обманывая иммунную систему пациента, заставляя распознавать злокачественные клетки меланомы, чтобы уничтожить их, как любого другого инородного захватчика. Хотя преимущества этой технологии все еще в значительной степени не определены, этот инструмент в настоящее время широко доступен через сертифицированных ветеринарных терапевтов и онкологов по всей территории США.
Настоятельно рекомендуется, чтобы владельцы, которые надеются добиться максимально комфортной продолжительности жизни своих питомцев, проконсультировались с сертифицированным онкологом, чтобы получить наиболее полное представление о широком спектре вариантов лечения своего питомца.
Как и в случае со многими другими агрессивными формами рака, лечение следует проводить быстро, поскольку злокачественные опухоли меланомы имеют тенденцию к быстрому распространению.
Ветеринарные расходы
Как и в случае со многими видами рака, требующими специализированной хирургии, передовых методов лечения рака и консультации онколога для достижения наилучших результатов, стоимость этого заболевания может оказаться непомерно высокой для многих владельцев домашних животных.
Домашние животные, страдающие агрессивными формами меланомы, могут столкнуться с расходами на лечение, значительно превышающими отметку в 10 000 долларов, особенно если владельцы решат изучить все доступные варианты лечения, включая новую вакцину от меланомы.
Стоимость окончательного диагноза обычно составляет около 500 долларов США или меньше, но резко возрастает, если владелец пациента решит исследовать опухоль и провести стадию для изучения вариантов лечения.
Химиотерапия: Стоимость химиотерапии в этих случаях варьируется в зависимости от размера пациента, но от 1000 до 3000 долларов считается типичной.
Хирургия: Стоимость самой операции будет зависеть от степени специализации хирурга и анатомического расположения опухоли, но от 2 000 до 5 000 долларов США типичны для агрессивной хирургии полости рта с вовлечением кости. При цене от 500 до 1000 долларов ампутация пальца ноги обычно обходится гораздо дешевле.
Радиация: Лучевая терапия в оральных случаях обычно стоит от 5000 до 10 000 долларов.
Вакцина: Сама вакцина стоит приблизительно от 1000 до 1500 долларов за дозу, при этом рекомендуется минимум четыре начальные дозы, а затем одна ревакцинация каждые шесть месяцев.
Невозможно переоценить тот факт, что стоимость диагностики и лечения зависит от многих факторов, включая географическое положение (стоимость жизни), уровень обслуживания (более низкие или более высокие стандарты ветеринарной помощи), наличие работы в специализированных больницах (более качественное оборудование, сертифицированный персонал и сертификаты для ветеринаров, специализирующихся в хирургии, внутренней медицине, онкологии и / или радиационной онкологии).
К сожалению, многие владельцы предпочитают не лечить домашних животных, пораженных более агрессивными формами меланомы, из-за чрезмерных расходов, часто связанных с этим заболеванием.
Профилактика
Как и в случае с большинством видов рака, нет известного подхода к профилактике меланомы.
Ссылки
Александр А.Н., Хуэльсмейер М.К., Митзи А. и др. Разработка вакцины против аллогенной цельноклеточной опухоли, экспрессирующей ксеногенный gp100, и ее реализация в клинических испытаниях фазы II на собаках со злокачественной меланомой. Cancer Immunol Immunother 2006; 55 (4): 433-442.
Бергман П.Дж., Кэмпс-Палау, Массачусетс, Макнайт Дж. А. и др. Разработка программы вакцинации ксеногенной ДНК от злокачественной меланомы собак в Ветеринарном центре.Vaccine 2006; 24 (21): 4582-4585.
Бергман П.Дж., Макнайт Дж., Новосад А. и др. Долгосрочное выживание собак с запущенной злокачественной меланомой после ДНК-вакцинации ксеногенной тирозиназой человека: испытание фазы I. Clin Cancer Res 2003; 9 (4): 1284-1290.
Модиано Дж. Ф., Ритт М. Г., Войчешин Дж. Молекулярные основы меланомы собак: патогенез и тенденции в диагностике и терапии. J Vet Intern Med 1999; 13 (3): 163-174.
Патнаик А.К., Муни С. Кошачья меланома: сравнительное исследование глазных, оральных и кожных новообразований.Vet Pathol 1988 25: 105.
Moore AS, Theilen GH, Newell AD, et al. Доклиническое исследование последовательного фактора некроза опухоли и интерлейкина 2 в лечении спонтанных новообразований у собак. Cancer Res 1991; 51 (1): 233-238.
Пру Д.Р., Русландер Д.М., Додж РК и др. Ретроспективный анализ 140 собак с меланомой ротовой полости, получавших дистанционное лучевое облучение. Vet Radiol Ultrasound 2003; 44 (3): 352-359.
Рамос-Вара Дж.А., Бейсенхерц М.Э., Миллер М.А. и др. Ретроспективное исследование 338 меланом ротовой полости собак с клиническим, гистологическим и иммуногистохимическим обзором 129 случаев.Ветеринарный патруль 2000; 37 (6): 597-608.

 Также на этой стадии меланома может быть не изъявлена, а её толщина может достигать от 1,01 до 2,00 мм. На этой стадии меланома ещё не поразила лимфатические узлы или дистальные органы.
Также на этой стадии меланома может быть не изъявлена, а её толщина может достигать от 1,01 до 2,00 мм. На этой стадии меланома ещё не поразила лимфатические узлы или дистальные органы. Меланома ещё не поразила лимфатические узлы или дистальные органы.
Меланома ещё не поразила лимфатические узлы или дистальные органы.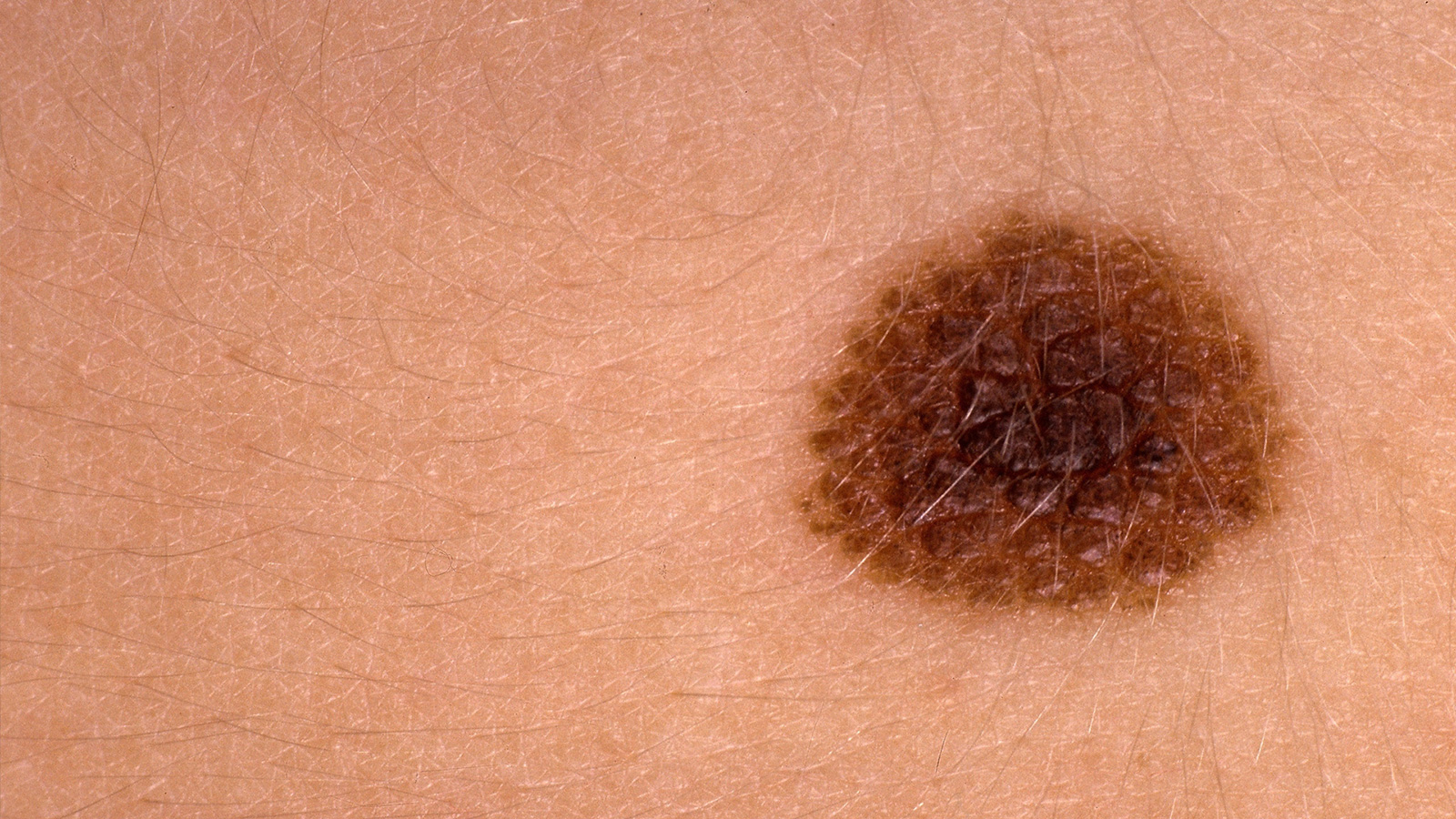 Лимфатические узлы – увеличены. Меланома ещё не распространилась на отдалённые участки.
Лимфатические узлы – увеличены. Меланома ещё не распространилась на отдалённые участки.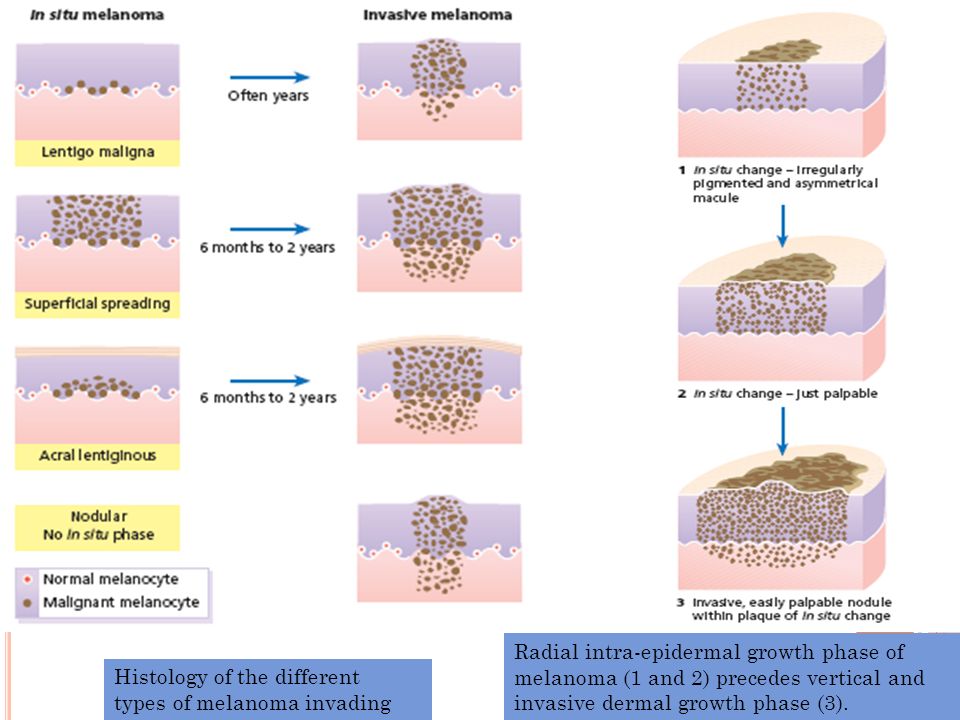 На отдалённые участки меланома также не распространилась.
На отдалённые участки меланома также не распространилась.