Лапароскопическое удаление кисты яичника: виды и способы операций, реабилитация
Услуги и цены
Удаление кист или кистом яичников, 4 койко-дней
75000 ₽
Лапароскопия хирургическая (стерилизация, удаление маточных труб или придатков (кроме тубоовариальных образований), удаление кист яичников менее 5 см в диаметре, удаление субсерозного миоматозного узла менее 5 см в диаметре), 3 койко-дня
85000 ₽
Пункция кисты яичника (без анестезиологического пособия)
12000 ₽
Первичный прием гинеколога
от 1700 ₽
Повторный прием гинеколога
от 1400 ₽
Первичный прием хирурга-гинеколога
2000 ₽
Повторный прием хирурга-гинеколога
1700 ₽
Киста — это опухолевидное образование, внутри которого содержится полость, заполненная жидкостью. Кисты яичника обнаруживаются достаточно часто, но большинство из них, порядка 85%, являются доброкачественными. Однако при исследовании женщин старше 50 лет примерно у половины выявляют признаки малигнизации. Любая киста требует наблюдения специалиста и тщательного инструментального обследования. Наиболее эффективный метод диагностики, который позволяет определить наличие кровотока — это УЗИ с допплерометрией.
Любая киста требует наблюдения специалиста и тщательного инструментального обследования. Наиболее эффективный метод диагностики, который позволяет определить наличие кровотока — это УЗИ с допплерометрией.
Кисты яичника, или доброкачественные опухолевидные образования, классифицируют на:
- функциональные,
- дермоидные,
- эндометриоидные,
- цистаденомы.
Функциональные кисты, в зависимости от структуры, участвующей в её образовании, подразделяют на фолликулярные и кисты желтого тела. Они формируются под действием изменяющегося уровня гормонов менструального цикла. Ежемесячно в яичнике созревает фолликул. Достигнув зрелости, он лопается. На его месте образуется желтое тело, а яйцеклетка продолжает свой путь. Так происходит в норме.
Фолликулярные кисты образуются из фолликула, который в ходе созревания не разорвался и остался в яичнике. В результате чего не произошло образования желтого тела, которое ответственно за выработку гормона прогестерона.
Киста желтого тела — это избыточное скопление жидкости на месте разорвавшегося фолликула. Женщина может заметить задержку менструации и другие вероятные признаки беременности.
Функциональные новообразования зачастую проходят самостоятельно в течение 3-6 месяцев. Однако требуют наблюдения со стороны специалиста, УЗИ-контроля и соблюдение рекомендаций врача. В отдельных случаях требуется назначение комбинированных оральных контрацептивов.
Эндометриоидная киста представляет собой полость, заполненную кровью. Новообразования такого типа возникают вследствие такого воспалительного заболевания, как эндометриоз, который распространился на яичники. Небольшие ежемесячные кровоизлияния из эндометриоидного очага сформировали кисту. Спустя время, кровь сворачивается и приобретает тягучую консистенцию и коричневый цвет. На макроскопическом исследовании содержимое кисты напоминает темный расплавленный шоколад.
Дермоидная киста относится к зрелым кистозным тератомам. Считается, что в ходе эмбрионального развития в яичник плода попадают клетки покровного эпителия, которые в норме там быть не должны. Дермоидные кисты обнаруживаются преимущественно у подростков или молодых женщин до 40 лет. Терас в переводе с греческого — чудовище. Такое название, вероятно, объясняется тем, что тератомы внутри, кроме жировой ткани, могут содержать также волосы, ногти, зубы и даже части более сложных органов.
Серозная киста (цистаденома) внешне схожа с фолликулярной. Однако имеет ряд особенностей, которые позволяют дифференцировать ее на УЗИ. Это важно, так как некоторые виды цистаденом имеют тенденцию к малигнизации. Серозные кисты можно разделить на простые и папиллярные. Последние характеризуются разрастаниями внутренней капсулы в виде сосочков, откуда и получили свое название. Папиллярная серозная киста в большинстве случаев перерождается в злокачественную опухоль. При подозрении на малигнизацию не проводят пункцию, вследствие того, что до 60% результатов являются ложноотрицательными.
Те или иные онкологические риски несут все новообразования яичника, за исключением функциональных, поэтому требуют оперативного лечения с последующим исследованием.
Это не значит, что все кисты должны быть немедленно удалены. Однако тяжелые спортивные нагрузки, неаккуратные половые отношения, травмы живота могут спровоцировать осложнения, что несет определенные риски.
- Перекрут ножки кисты приводит к сдавлению нервов и сосудов, питающих ее. Это влечет за собой развитие некротических процессов. У женщин полость малого таза сообщается с брюшной, поэтому процессы разложения и воспаления затрагивают брюшину с развитием перитонита. Клинически перекрут ножки кисты проявляется схваткообразными болями в животе, учащенным сердцебиением, повышением температуры тела, рвотой, тошнотой.
- Нагноение кисты происходит при присоединении вторичной бактериальной инфекции, причиной которой могут быть инфекционные заболевания органов малого таза.
 Процесс сопровождается клиникой острого живота, лихорадкой, развитием перитонита.
Процесс сопровождается клиникой острого живота, лихорадкой, развитием перитонита.
- Разрыв кисты, пожалуй, представляет самое тяжелое осложнение. Содержимое кисты выходит в полость малого таза, которая у женщин сообщается с брюшной полостью, вызывая перитонит.
Часто разрыв кисты вызывает кровотечение, сопровождающееся чрезвычайно сильной болью в животе, тахикардией и потерей сознания.
Развитие осложнений является показанием к экстренному оперативному вмешательству.
Показания к удалению.
Чаще всего функциональные кисты не нуждаются в хирургическом удалении. Они не имеют тенденцию к малигнизации, а значит, не несут онкологических рисков. Функциональные кисты проходят сами, либо пациентам назначается гормональная терапия оральными контрацептивами, которые приостанавливают цикл, и связанные с ним новообразования редуцируются. Однако, если консервативная терапия оказалась безуспешна и не подходит по каким-либо причинам, производят хирургическое удаление кисты.
Хирургическое лечение показано при обнаружении любого новообразования яичника в менопаузу, неэффективности консервативной терапии более 3-х месяцев, в случае функциональных кист и при наличии риска малигнизации. Развитие любого из осложнений (нагноение, кровоизлияние, разрыв, перекрут ножки) — это показание для оперативного вмешательства в экстренном порядке.
Объем резекции и выбор доступа определяется индивидуально вместе с пациенткой до операции. Также до вмешательства необходимо проговорить варианты резекции, которые могут быть при обнаружении злокачественности новообразования.
В настоящее время большинство плановых операций выполняются с использованием лапароскопического доступа, снижающего травматизацию тканей, выраженность болевого синдрома и время реабилитации.
Как проходит операция
В зависимости от типа новообразования хирург выбирает оперативную тактику. Начинают с ревизии органов малого таза — оценивают состояние тканей, наличие выпота, находят новообразование.
Цистэктомия — удаление непосредственно самой кисты без захвата рядом расположенных органов и структур. Новообразование аккуратно отделяют от прилежащих тканей. Случайное вскрытие кисты и излитие ее содержимого могут привести к перитониту. Удаленный материал помещают в специальный контейнер. После извлечения кисту вскрывают и внимательно осматривают. Проверяют содержимое и стенки капсулы.
Подготовка к операции
Подготовка начинается с проведения инструментальной диагностики — УЗИ (трансвагинальное и абдоминальное), допплерография. При подозрении на распространенный онкологический процесс может быть назначены МРТ или КТ. Проводится лабораторная диагностика, включающая в себя стандартный набор анализов на инфекции, свертываемость крови и воспалительные маркеры. В некоторых случаях дополнительно назначается сдача крови на онкомаркеры. От грамотной подготовки и полученных результатов будет зависеть объем вмешательства. Как и при любом другом оперативном вмешательстве, накануне ограничивается прием пищи, а с утра — воды.
Реабилитационный период
После лапароскопии реабилитационный период короче, чем при традиционных оперативных вмешательствах. Применяют принцип ранней активизации с 1-х суток. А выписка производится уже на 2-3 сутки. К полноценной жизни без ограничений рекомендуют возвращаться через 6-8 недель. До этого срока стоит придерживаться щадящего режима физических нагрузок и полового покоя. На протяжении года потребуется проходить контрольные обследования: УЗИ и бимануальное исследование.
Применяют принцип ранней активизации с 1-х суток. А выписка производится уже на 2-3 сутки. К полноценной жизни без ограничений рекомендуют возвращаться через 6-8 недель. До этого срока стоит придерживаться щадящего режима физических нагрузок и полового покоя. На протяжении года потребуется проходить контрольные обследования: УЗИ и бимануальное исследование.
Беременность после лапароскопии
Сам по себе лапароскопический доступ не несет риска для будущей беременности, так как не происходит травматизации эпителия матки. Сохранность репродуктивной функции зависит от объема вмешательства. При сохранной функции яичников и целостности маточных труб удаление кисты не несет рисков, связанных с бесплодием.
Назад к списку статей
факторы риска и профилактика uMEDp
Статья посвящена одному из наиболее обсуждаемых вопросов в современной гинекологии – проблеме рецидивирования эндометриоидных кист. Рассматриваются факторы риска развития рецидива, особенности эндометриоидных кист, склонных к рецидиву, а также принципы гормональной терапии в послеоперационном периоде. Отмечается целесообразность проведения гистологической оценки типа эндометриоидных кист, иммуногистохимического исследования с определением уровня экспрессии маркеров пролиферации, апоптоза и неоангиогенеза. Некоторые перспективы связываются с поиском генов, сопряженных с риском возникновения рецидивов эндометриоидных кист.
Отмечается целесообразность проведения гистологической оценки типа эндометриоидных кист, иммуногистохимического исследования с определением уровня экспрессии маркеров пролиферации, апоптоза и неоангиогенеза. Некоторые перспективы связываются с поиском генов, сопряженных с риском возникновения рецидивов эндометриоидных кист.
Как известно, наиболее частое диагностируемое проявление эндометриоза – это эндометриоидные кисты (ЭК) яичников. Их обнаруживают у 10–14% женщин, оперированных по поводу различных объемных образований органов малого таза.
Частота возникновения рецидивов эндометриоза после хирургического лечения через один-два года составляет 15–21%, в течение двух – пяти лет при адекватном удалении очагов – 12–30%, спустя пять лет – 36–47%, а через пять – семь лет – 50–55%.
Чаще всего рецидив наблюдается при распространенном эндометриозе или невозможности удалить инфильтративные очаги в органах репродуктивной системы (узловые формы аденомиоза, ретроцервикальный эндометриоз с частичным или полным прорастанием стенки прямой или сигмовидной кишки, дистальных отделов мочеточников, мочевого пузыря и т. д.). Однако в этих случаях клиническое течение целесообразно квалифицировать как прогрессирование заболевания, а не рецидив [1].
д.). Однако в этих случаях клиническое течение целесообразно квалифицировать как прогрессирование заболевания, а не рецидив [1].
Факторы риска развития рецидива эндометриоидных кист
Существует множество факторов и особенностей течения болезни, по которым можно прогнозировать риск развития рецидива ЭК.
Наследственность. Риск развития рецидивирующего типа ЭК повышен, если у ближайших родственниц (чаще по материнской линии) были злокачественные и доброкачественные заболевания гениталий, а также экстрагенитальные опухоли [2, 3]. Имеет значение и генетический фактор. Эпигенетические изменения в эндометриальных стволовых клетках, предназначенных для формирования различных органов и тканей малого таза, негативно влияют на экспрессию генов, которые кодируют стероидогенный фактор 1 и эстрогеновый рецептор бета. Эти эпигенетические изменения включают так называемое деметилирование – активацию и чрезмерную экспрессию стероидогенного фактора 1 и эстрогенового рецептора бета, играющих ключевую роль в патогенезе эндометриоза. Полагают, что генетическая предрасположенность к чрезмерной продукции стероидогенного фактора 1 и эстрогенового рецептора бета может приводить к развитию эндометриоза у женщин в любом возрасте. В ответ на воздействие провоспалительных веществ, особенно простагландина Е2, стероидогенный фактор 1 связывается в эндометриоидных клетках со многими стероидогенными генами, включая ген ароматазы, следствием чего становится усиление образования эстрадиола. Эстрадиол с помощью эстрогенового рецептора бета стимулирует активность фермента циклооксигеназы типа 2, способствуя гиперпродукции простагландина Е2. Связывание эстрогенового рецептора бета с промоторной зоной прогестероновых рецепторов снижает их экспрессию, становясь одной из причин развития резистентности к прогестерону [1].
Полагают, что генетическая предрасположенность к чрезмерной продукции стероидогенного фактора 1 и эстрогенового рецептора бета может приводить к развитию эндометриоза у женщин в любом возрасте. В ответ на воздействие провоспалительных веществ, особенно простагландина Е2, стероидогенный фактор 1 связывается в эндометриоидных клетках со многими стероидогенными генами, включая ген ароматазы, следствием чего становится усиление образования эстрадиола. Эстрадиол с помощью эстрогенового рецептора бета стимулирует активность фермента циклооксигеназы типа 2, способствуя гиперпродукции простагландина Е2. Связывание эстрогенового рецептора бета с промоторной зоной прогестероновых рецепторов снижает их экспрессию, становясь одной из причин развития резистентности к прогестерону [1].
Инфекционный фактор. У пациенток с рецидивирующим типом эндометриоза яичников в анамнезе часто имеется указание на хронический тонзиллит, перенесенные детские инфекции, такие как корь, скарлатина. Известно, что инфекционно-токсические заболевания оказывают опосредованное повреждающее действие на репродуктивную систему, снижая устойчивость организма к различным патогенным факторам и создавая фон для развития стойких метаболических нарушений [3].
Известно, что инфекционно-токсические заболевания оказывают опосредованное повреждающее действие на репродуктивную систему, снижая устойчивость организма к различным патогенным факторам и создавая фон для развития стойких метаболических нарушений [3].
Экстрагенитальная патология. Следует отметить, что у пациенток с рецидивами ЭК имеет место более выраженный характер экстрагенитальной патологии [4, 5]. В ее структуре преобладают заболевания сердечно-сосудистой системы (17,3%), щитовидной железы (16,3%), желудочно-кишечного тракта (14,5%), гепатобилиарного комплекса (14,5%), центральной нервной системы (0,9%) [2]. Доказано, что слизистая желудка и кишечника способна синтезировать биологически активные вещества и гормональные соединения, инактивировать микробные и химические токсины, принимает участие в обеспечении иммунного ответа. В этой связи хронические заболевания органов желудочно-кишечного тракта сопровождаются замедлением метаболизма, что в свою очередь провоцирует пролиферативные изменения в органах-мишенях, в том числе в яичниках.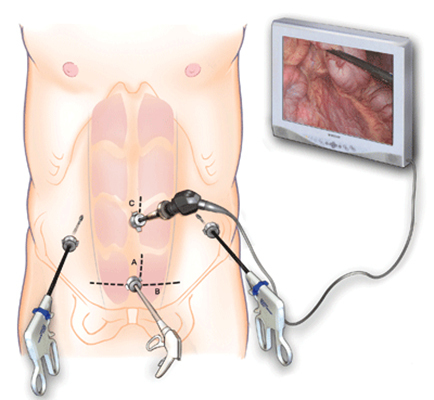 Патология гепатобилиарного тракта способствует конъюгации эстрогенов и повышению уровня свободных эстрогенов. Это приводит к возникновению печеночной гиперэстрогении, которая может способствовать развитию дисгормональной гиперплазии в органах репродуктивной системы. Часто рецидивы ЭК сочетаются с ожирением и сахарным диабетом. Это объясняется развитием инсулинорезистентности и гиперинсулинемии, которая способствует уменьшению синтеза в печени стероидсвязывающего глобулина, необходимого для выведения избыточных андрогенов. В условиях развития гиперандрогении усиливается активность фермента ароматазы и формируется гиперэстрогения – еще одно звено патогенеза эндометриоза [1].
Патология гепатобилиарного тракта способствует конъюгации эстрогенов и повышению уровня свободных эстрогенов. Это приводит к возникновению печеночной гиперэстрогении, которая может способствовать развитию дисгормональной гиперплазии в органах репродуктивной системы. Часто рецидивы ЭК сочетаются с ожирением и сахарным диабетом. Это объясняется развитием инсулинорезистентности и гиперинсулинемии, которая способствует уменьшению синтеза в печени стероидсвязывающего глобулина, необходимого для выведения избыточных андрогенов. В условиях развития гиперандрогении усиливается активность фермента ароматазы и формируется гиперэстрогения – еще одно звено патогенеза эндометриоза [1].
Отягощенный акушерско-гинекологический анамнез. У пациенток с рецидивами ЭК часто имеются указания на длительное бесплодие, медицинские аборты, самопроизвольные выкидыши [4]. В условиях многократно повторяющихся менструальных циклов менструальный рефлюкс (попадание некоторого количества эндометриальных клеток в брюшную полость через маточные трубы) становится универсальным фактором агрессии, ведет к резкому ослаблению иммунной системы и возникновению неадекватного ответа. Кроме того, в анамнезе рецидивирующие ЭК часто сочетаются с гиперпластическими процессами эндометрия, клинически активным аденомиозом, миомой матки, хроническими воспалительными заболеваниями (эндометритом, аднекситом). Это связано с общностью патогенетических факторов: гиперэстрогенией, резистентностью к прогестерону, нарушением процессов апоптоза, накоплением провоспалительных факторов, нарушением соотношения простагландинов.
Кроме того, в анамнезе рецидивирующие ЭК часто сочетаются с гиперпластическими процессами эндометрия, клинически активным аденомиозом, миомой матки, хроническими воспалительными заболеваниями (эндометритом, аднекситом). Это связано с общностью патогенетических факторов: гиперэстрогенией, резистентностью к прогестерону, нарушением процессов апоптоза, накоплением провоспалительных факторов, нарушением соотношения простагландинов.
Клиническое течение. Для ЭК, склонных к рецидиву, характерны более выраженные клинические симптомы: гиперполименорея (65,1%), дисменорея (82,6%), диспареуния (82,6%) [2, 3]. При нерецидивирующем течении эти нарушения встречаются с частотой 8,2, 7,1, 15,3% соответственно. В половине случаев нерецидивирующих ЭК клинические проявления заболевания отсутствуют, а образования случайно обнаруживаются при проведении ультразвукового исследования. Существует мнение, что выраженность клинических симптомов коррелирует со степенью сосудистых нарушений, а также с наличием ЭК, инфильтративными формами эндометриоза и спаечным процессом малого таза. К наиболее частым признакам рецидивирующих ЭК относятся возобновление болевого синдрома и повышение уровня онкомаркера СА-125 в крови [2, 6].
К наиболее частым признакам рецидивирующих ЭК относятся возобновление болевого синдрома и повышение уровня онкомаркера СА-125 в крови [2, 6].
Особенности эндометриоидных кист, склонных к рецидиву
При проведении дополнительных методов исследования выявлены следующие особенности ЭК, склонных к рецидиву.
Ультразвуковые критерии. Для ЭК, склонных к рецидиву, характерен умеренный и выраженный кровоток практически во всех отделах кисты. При этом максимальная скорость артериального кровотока достоверно выше, чем при нерецидивирующем варианте ЭК [3].
Лапароскопическая диагностика. Рецидивирующие ЭК в 100% случаев сочетаются с перитонеальным эндометриозом [7], в то время как нерецидивирующие – только в 38% случаев [3]. Кроме того, при рецидивирующем течении заболевания спаечный процесс той или иной степени обнаруживается у всех пациенток, а поверхностные эндометриоидные образования яичников – у 28,8% [8].
Морфология. В настоящее время выделяют два вида ЭК: железисто-кистозный и кистозный. Железисто-кистозный вариант характеризуется наличием в стенке многочисленных желез и цитогенной стромы с разнообразными клеточными элементами, эпителием пролиферирующего типа, большим количеством артериол с тонкой гладкомышечной стенкой. Для кистозного варианта характерны отсутствие желез, фиброзированная строма, а также фиброзный и дистрофический эпителий, в стенке кисты определяются отдельные сосуды с утолщенными склерозированными стенками [9].
Существует мнение, что на основании изучения жалоб больной, данных ультразвукового исследования с цветным допплеровским картированием, определения уровня маркера СА-125 возможно предположить морфологический тип ЭК на дооперационном этапе. Так, железисто-кистозной форме свойственны незначительные размеры кисты, как правило не превышающие 4 см, наличие тонкой стенки, отсутствие четкой границы между новообразованием и здоровой яичниковой тканью, активная васкуляризация. При цветном допплеровском картировании регистрируются средняя скорость кровотока и низкие индексы периферического сосудистого сопротивления. В то время как у пациенток с кистозным вариантом образования имеют место размеры образования от 4,4 до 12 см, двойной контур, единичные локусы кровотока в области ворот, а в большинстве случаев кистозное образование аваскулярно. Кроме того, железисто-кистозный тип в 100% случаев сочетается со спаечным процессом, а также с эндометриоидными гетеротопиями инфильтративного характера. Следует отметить, что для пациенток с железисто-кистозной формой характерен более высокий уровень маркера СА-125 (в среднем 149,2 Ед/мл), в то время как у женщин с кистозным типом он колеблется в среднем на уровне 26,5 Ед/мл. Клиническая симптоматика более выражена при железисто-кистозном варианте [7, 9].
При цветном допплеровском картировании регистрируются средняя скорость кровотока и низкие индексы периферического сосудистого сопротивления. В то время как у пациенток с кистозным вариантом образования имеют место размеры образования от 4,4 до 12 см, двойной контур, единичные локусы кровотока в области ворот, а в большинстве случаев кистозное образование аваскулярно. Кроме того, железисто-кистозный тип в 100% случаев сочетается со спаечным процессом, а также с эндометриоидными гетеротопиями инфильтративного характера. Следует отметить, что для пациенток с железисто-кистозной формой характерен более высокий уровень маркера СА-125 (в среднем 149,2 Ед/мл), в то время как у женщин с кистозным типом он колеблется в среднем на уровне 26,5 Ед/мл. Клиническая симптоматика более выражена при железисто-кистозном варианте [7, 9].
Локализация и объем выполненного оперативного вмешательства. Рецидив чаще наблюдается у пациенток, перенесших двусторонние органосохраняющие операции и одностороннюю аднексэктомию [9, 10, 11].
Иммуногистохимическое исследование. У пациенток с рецидивирующим типом ЭК уровень маркера пролиферации Кi-67 повышен, экспрессия проапоптотического фактора СБ-95 низкая. Иначе говоря, есть основание считать, что очаги эндометриоза яичников образуются из клеток эндометрия с высоким пролиферативным потенциалом и низким уровнем апоптоза. В строме рецидивирующих ЭК отмечаются усиление неоангиогенеза и повышение экспрессии факторов роста, что приводит к более выраженному неоангиогенезу и инвазии эндометриоидных гетеротопий, а в последующем к развитию кровоизлияний в просвет образования и формированию полости кисты.
Гормональная терапия в послеоперационном периоде
Следует отметить, что гормональная терапия в послеоперационном периоде должна осуществляться дифференцированно с учетом репродуктивных планов пациентки [1]. Консервативная терапия агонистами гонадотропин-рилизинг гормона имеет преимущества: она восстанавливает репродуктивную функцию у больных эндометриозом, позволяет в некоторых случаях отказаться от выполнения радикальных операций, улучшает результаты консервативной терапии и качество жизни пациенток. Одной из особенностей применения агонистов гонадотропин-рилизинг гормона является rebound-эффект – после отмены терапии происходит активация гипоталамо-гипофизарно-яичниковой системы, стимуляция овуляции и повышается вероятность наступления беременности [12, 13]. Кроме того, агонисты гонадотропин-рилизинг гормона оказывают протективное действие, защищая недифференцированные герминогенные стволовые клетки, которые генерируют примордиальные фолликулы, сохраняют большой пул «дремлющих» примордиальных фолликулов, а также снижают синтез примордиального ростового фактора фолликулами, зависимыми от фолликулостимулирующего гормона [14].
Одной из особенностей применения агонистов гонадотропин-рилизинг гормона является rebound-эффект – после отмены терапии происходит активация гипоталамо-гипофизарно-яичниковой системы, стимуляция овуляции и повышается вероятность наступления беременности [12, 13]. Кроме того, агонисты гонадотропин-рилизинг гормона оказывают протективное действие, защищая недифференцированные герминогенные стволовые клетки, которые генерируют примордиальные фолликулы, сохраняют большой пул «дремлющих» примордиальных фолликулов, а также снижают синтез примордиального ростового фактора фолликулами, зависимыми от фолликулостимулирующего гормона [14].
Данные метаанализа 2010 г., в который вошли три рандомизированных клинических исследования (n = 165), показал, что назначение пациенткам с эндометриозом перед проведением программ вспомогательных репродуктивных технологий агонистов гонадотропин-рилизинг гормона с целью супрессии на срок от трех до шести месяцев повышает шансы наступления клинической беременности более чем в 4 раза [15].
Показаниями к терапии эндометриоза отечественным агонистом гонадотропин-рилизинг гормона Бусерелином-лонг ФС являются:
- распространенный эндометриоз (средней или тяжелой степени) до и/или после хирургического лечения;
- эндометриоз легкой степени и бесплодие после проведения хирургического лечения;
- эндометриоз любой степени тяжести при наличии клинических симптомов после хирургического лечения;
- отказ пациентки от операции;
- невозможность проведения хирургического лечения;
- отсутствие эффекта от назначения комбинированных оральных контрацептивов или прогестагенов.
В настоящее время существуют новые подходы к гормональной терапии эндометриоза, а именно применение препарата Бусерелин-лонг ФС с последующим длительным назначением диеногеста или приемом низкодозированных комбинированных контрацептивов в пролонгированном режиме.
Существует мнение, что комбинированные оральные контрацептивы не эффективны для лечения рецидива ЭК, поскольку эндометриоз является эстрогензависимым заболеванием, а комбинированные оральные контрацептивы содержат эстрогенный компонент, вследствие чего нельзя исключить потенциальную стимуляцию развития, прогрессирования и рецидивирования заболевания [1]. В этой связи комбинированные оральные контрацептивы следует назначать в непрерывном режиме для исключения пиков эстрогенов, а также для устранения симптомов эндометриоза. Некоторые авторы рекомендуют вместе с комбинированными оральными контрацептивами использовать диосмин (Флебодиа 600) для снижения выраженности гормонзависимой боли, поскольку эстрогены стимулируют выработку оксида азота и опосредованно способствуют расширению вен. Прогестагены также оказывают сосудорасширяющий эффект и могут усиливать боль при варикозном расширении вен нижних конечностей и малого таза [16, 17].
В этой связи комбинированные оральные контрацептивы следует назначать в непрерывном режиме для исключения пиков эстрогенов, а также для устранения симптомов эндометриоза. Некоторые авторы рекомендуют вместе с комбинированными оральными контрацептивами использовать диосмин (Флебодиа 600) для снижения выраженности гормонзависимой боли, поскольку эстрогены стимулируют выработку оксида азота и опосредованно способствуют расширению вен. Прогестагены также оказывают сосудорасширяющий эффект и могут усиливать боль при варикозном расширении вен нижних конечностей и малого таза [16, 17].
Эндометриоидные кисты: клиническая практика
Нами проведен ретроспективный анализ медицинской документации за последние пять лет. Всего были изучены данные 121 пациентки, прооперированной в клинике по поводу ЭК яичников, в том числе 19 случаев в связи с рецидивами.
Оказалось, что соматический анамнез был отягощен в подавляющем большинстве случаев, причем превалировали патология желудочно-кишечного тракта и аутоиммунные заболевания. У всех пациенток с рецидивом ЭК в анамнезе имелись указания на частые инфекционные заболевания и наличие очагов хронической инфекции. В 70% случаев репродуктивный анамнез был отягощен бесплодием и невынашиванием беременности.
У всех пациенток с рецидивом ЭК в анамнезе имелись указания на частые инфекционные заболевания и наличие очагов хронической инфекции. В 70% случаев репродуктивный анамнез был отягощен бесплодием и невынашиванием беременности.
У подавляющего большинства пациенток с рецидивами ЭК перед операцией наблюдалась выраженная клиническая картина заболевания, в которой превалировал болевой синдром.
У всех пациенток с рецидивами ЭК имели место органосохраняющие операции, при этом выявлено сочетание ЭК с эндометриоидными гетеротопиями по брюшине малого таза и спаечным процессом.
В послеоперационном периоде 26% пациенток с рецидивами ЭК не получали гормонального лечения.
12 пациенткам с рецидивирующей ЭК диаметром 5 см и более было проведено повторное хирургическое органосохраняющее вмешательство, в 11 случаях – кистэктомия, в одном – аднексэктомия с одной стороны и резекция с другой.
У семи пациенток с рецидивом ЭК (кисты меньше 3 см в диаметре) и планирующим беременность в ближайшее время вопрос об оперативном вмешательстве был решен отрицательно в связи с большим риском истощения яичников. С учетом протективного в отношении яичников эффекта и способности агонистов гонадотропин-рилизинг гормона повышать вероятность наступления беременности при эндометриозе этим пациенткам была рекомендована патогенетическая терапия препаратом Бусерелин-лонг ФС на протяжении трех месяцев.
С учетом протективного в отношении яичников эффекта и способности агонистов гонадотропин-рилизинг гормона повышать вероятность наступления беременности при эндометриозе этим пациенткам была рекомендована патогенетическая терапия препаратом Бусерелин-лонг ФС на протяжении трех месяцев.
Заключение
Основываясь на данных литературы о факторах риска рецидива ЭК, мы полагаем, что в каждом случае в прогностических целях следует проводить гистологическую оценку типа ЭК (кистозный или железисто-кистозный вариант), иммуногистохимическое исследование с оценкой уровня экспрессии маркеров пролиферации, апоптоза и неоангиогенеза. В перспективе после оперативного лечения необходим поиск генов, сопряженных с риском возникновения рецидивов ЭК. Это позволит не откладывать наступление беременности у женщин репродуктивного возраста после операции и безотлагательно решать вопрос о вспомогательных репродуктивных технологиях. При генетическом риске рецидива ЭК у женщин с реализованной репродуктивной функцией, по-видимому, целесообразно расширять объем оперативного вмешательства, возможно даже до радикальной операции.
Послеоперационная гормональная терапия для предотвращения рецидива эндометриомы после цистэктомии яичников: систематический обзор и сетевой метаанализ
Метаанализ
. 2021 Январь; 128(1):25-35.
дои: 10.1111/1471-0528.16366. Epub 2020 14 июля.
Р Ваттанаингчароенчай 1 2 , С. Ратанасири 1 , К Чаракорн 1 2 , Дж Аттиа 3 , Таккинстианец 1
Принадлежности
- 1 Отделение клинической эпидемиологии и биостатистики, медицинский факультет больницы Раматибоди, Университет Махидол, Бангкок, Таиланд.

- 2 Кафедра акушерства и гинекологии, больница Раматибоди медицинского факультета, Университет Махидол, Бангкок, Таиланд.
- 3 Центр клинической эпидемиологии и биостатистики, Школа медицины и общественного здравоохранения, факультет здравоохранения и медицины, Университет Ньюкасла, Нью-Лэмбтон, Австралия.
- PMID: 32558987
- PMCID: PMC7754428
- DOI: 10.1111/1471-0528.16366
Бесплатная статья ЧВК
Метаанализ
R Wattanayingcharoenchai et al. БЖОГ.
2021 9 января0003
БЖОГ.
2021 9 января0003
Бесплатная статья ЧВК
. 2021 Январь; 128(1):25-35.
дои: 10.1111/1471-0528.16366. Epub 2020 14 июля.
Авторы
Р Ваттанайингчароенчай 1 2 , Южный Ратанасири 1 , К Чаракорн 1 2 , Дж Аттиа 3 , Таккинстианец 1
Принадлежности
- 1 Отделение клинической эпидемиологии и биостатистики, медицинский факультет больницы Раматибоди, Университет Махидол, Бангкок, Таиланд.
- 2 Кафедра акушерства и гинекологии, больница Раматибоди медицинского факультета, Университет Махидол, Бангкок, Таиланд.
- 3 Центр клинической эпидемиологии и биостатистики, Школа медицины и общественного здравоохранения, факультет здравоохранения и медицины, Университет Ньюкасла, Нью-Лэмбтон, Австралия.
- PMID: 32558987
- PMCID: PMC7754428
- DOI: 10.1111/1471-0528.16366
Абстрактный
Фон: Эффективность гормональных схем для профилактики рецидива эндометриомы у женщин, перенесших консервативное хирургическое вмешательство, до сих пор остается спорной.
Задача: Сравнить эффективность различных гормональных режимов в этом контексте и ранжировать их.
Стратегия поиска: Поиск в базах данных MEDLINE и Scopus проводился до января 2020 года.
Критерий выбора: Рандомизированные контролируемые испытания (РКИ) или когорты, сравнивающие эффект любой пары вмешательств (например, циклические оральные контрацептивы [ОК], непрерывный прием ОК, агонисты гонадотропин-рилизинг гормона [ГнРГ], диеногест [ДНГ], левоноргестрел-рилизинг внутриматочная система [ЛНГ] -IUS] и выжидательная тактика) при рецидиве эндометриомы.
Сбор и анализ данных: Данные были независимо извлечены двумя рецензентами. Относительные эффекты лечения оценивали с помощью сетевого метаанализа (NMA) и ранжировали в порядке убывания.
Основные результаты: Были включены шесть РКИ (675 пациентов) и 16 когорт (3089 пациентов). NMA РКИ, включающих выжидательную тактику, циклические ОК, непрерывные ОК, аГнРГ и аГнРГ + ЛНГ-ВМС, показала, что все гормональные схемы имели незначительно более низкий риск рецидива эндометриомы по сравнению с выжидательной тактикой. NMA когорт, включающих выжидательную, циклическую ОК, непрерывную ОК, аГнРГ, ДНГ, ЛНГ-ВМС, аГнРГ + ОК и аГнРГ + ЛНГ-ВМУ, показала, что ЛНГ-ВМС, ДНГ, непрерывная ОК, аГнРГ + ОК и циклическая ОК имели значительно более низкий риск рецидива эндометриомы, чем выжидательная тактика. ЛНГ-ВМС заняла первое место, за ним следуют ДНГ и ГнРГ + ЛНГ-ВМС. Длительное использование гормональной терапии ОК или прогестинами имело значительно более низкий риск рецидива эндометриомы, чем ожидаемое лечение.
Вывод: В NMA РКИ не было доказательств в поддержку гормональной терапии для послеоперационной профилактики рецидива эндометриомы. Это противоречило когортным данным, в которых был обнаружен защитный эффект ОК и режимов прогестина, особенно при длительном лечении. По-прежнему требуются крупномасштабные РКИ этих агентов.
Это противоречило когортным данным, в которых был обнаружен защитный эффект ОК и режимов прогестина, особенно при длительном лечении. По-прежнему требуются крупномасштабные РКИ этих агентов.
Резюме для твиттера: Гормональные схемы, назначаемые в качестве длительного лечения, имеют тенденцию снижать риск рецидива эндометриомы после консервативной хирургии.
Ключевые слова: эндометриома; гормональное лечение; сетевой метаанализ; цистэктомия яичников; повторение.
© 2020 Авторы. BJOG: Международный журнал акушерства и гинекологии, издаваемый John Wiley & Sons Ltd от имени Королевского колледжа акушеров и гинекологов.
Цифры
Рисунок 1
Блок-схема выбора исследования.
Рисунок 1
Блок-схема выбора исследования.
фигура 1Блок-схема выбора исследования.
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Поддерживающая терапия для предотвращения рецидива эндометриомы после операции по резекции эндометриоза — систематический обзор и сетевой метаанализ.
Чиу К.С., Хсу Т.Ф., Цзян Л.И., Чан И.С., Ши Ю.К., Чанг Ю.Х., Ван П.Х., Чен Ю.Дж. Чиу С.С. и др. J Миним инвазивный гинекол. 2022 май; 29(5):602-612. doi: 10.1016/j.jmig.2021.11.024. Epub 2022 2 фев. J Миним инвазивный гинекол. 2022. PMID: 35123042 Обзор.
Послеоперационная внутриматочная система, высвобождающая левоноргестрел, по сравнению с оральными контрацептивами после лечения агонистами гонадотропин-высвобождающего гормона для предотвращения рецидива эндометриомы.

Чо С., Чон Дж. А., Ли И., Ким Х.И., Сео С.К., Чхве Ю.С., Ли Д.С., Ли Б.С. Чо С. и др. Acta Obstet Gynecol Scand. 2014 Январь; 93 (1): 38-44. дои: 10.1111/аогс.12294. Acta Obstet Gynecol Scand. 2014. PMID: 24605384
Варианты профилактической терапии послеоперационного рецидива эндометриомы яичников: агонисты гонадотропин-рилизинг-гормона с введением или без введения внутриматочной системы левоноргестрела.
Zhu SY, Wu YS, Gu ZY, Zhang J, Jia SZ, Shi JH, Dai Y, Leng JH, Li XY. Чжу С.И. и др. Arch Gynecol Obstet. 2021 фев; 303 (2): 533-539. doi: 10.1007/s00404-020-05843-5. Epub 2020 26 октября. Arch Gynecol Obstet. 2021. PMID: 33104866
Хирургия против медикаментозной терапии обильных менструальных кровотечений.

Марджорибанкс Дж., Летаби А., Фаркуар С. Марджорибанкс Дж. и др. Cochrane Database Syst Rev. 2016 29 января; 2016(1):CD003855. doi: 10.1002/14651858.CD003855.pub3. Кокрановская система базы данных, ред. 2016 г. PMID: 26820670 Бесплатная статья ЧВК. Обзор.
Внутриматочная спираль, высвобождающая левоноргестрел (ЛНГ-ВМС), при симптоматическом эндометриозе после операции.
Abou-Setta AM, Al-Inany HG, Farquhar CM. Абу-Сетта А.М. и соавт. Cochrane Database Syst Rev. 2006 Oct 18;(4):CD005072. doi: 10.1002/14651858.CD005072.pub2. Кокрановская система базы данных, ред. 2006 г. PMID: 17054236 Обновлено. Обзор.
Посмотреть все похожие статьи
Цитируется
Идентификация функциональной регуляторной сети гена TF-miRNA-hub, связанной с эндометриозом яичников.

Ли Л., Сун Б., Сун Ю. Ли Л и др. Фронт Жене. 2022 сен 20;13:998417. doi: 10.3389/fgene.2022.998417. Электронная коллекция 2022. Фронт Жене. 2022. PMID: 36212136 Бесплатная статья ЧВК.
Разработка прогностической номограммы рецидива у пациенток с эндометриомой после цистэктомии в возрасте до 45 лет, получавших послеоперационную терапию.
Gu Z, Li X, Shi J, Wu Y, Zhang J, Zhang C, Yan H, Leng J. Гу Зи и др. Front Med (Лозанна). 2022 9 июня; 9:872481. doi: 10.3389/fmed.2022.872481. Электронная коллекция 2022. Front Med (Лозанна). 2022. PMID: 35755050 Бесплатная статья ЧВК.
Долгосрочная эффективность и безопасность внутриматочной системы, высвобождающей левоноргестрел, в качестве поддерживающей терапии эндометриоза.

Kim HY, Song SY, Jung SH, Song HJ, Lee M, Lee KH, Jung YW, Yoo HJ. Ким ХИ и др. Медицина (Балтимор). 2022 11 марта; 101 (10): e29023. doi: 10.1097/MD.0000000000029023. Медицина (Балтимор). 2022. PMID: 35451403 Бесплатная статья ЧВК.
Внешний аденомиоз связан с послеоперационным рецидивом эндометриомы яичников.
Сунь М., Сюй П., Цзоу Г., Ван Дж., Чжу Л., Чжан С. Сан М. и др. Front Med (Лозанна). 2022 12 января; 8:815628. doi: 10.3389/fmed.2021.815628. Электронная коллекция 2021. Front Med (Лозанна). 2022. PMID: 35096905 Бесплатная статья ЧВК.
Факторы риска рецидива эндометриомы яичника после хирургического удаления: систематический обзор и метаанализ.
Цзян Д., Чжан С.
 , Ши Дж., Тао Д., Не С.
Цзян Д. и др.
Arch Gynecol Obstet. 2021 сен; 304 (3): 589-598. doi: 10.1007/s00404-021-06129-0. Epub 2021 20 июня.
Arch Gynecol Obstet. 2021.
PMID: 34148122
Обзор.
, Ши Дж., Тао Д., Не С.
Цзян Д. и др.
Arch Gynecol Obstet. 2021 сен; 304 (3): 589-598. doi: 10.1007/s00404-021-06129-0. Epub 2021 20 июня.
Arch Gynecol Obstet. 2021.
PMID: 34148122
Обзор.
Просмотреть все статьи «Цитируется по»
использованная литература
- Лю С, Юань Л, Шен Ф, Чжу З, Цзян Х, Го С.В. Паттерны и факторы риска рецидивов у женщин с эндометриомами яичников. Obstet Gynecol 2007;109:1411–20. — пабмед
- Хики М., Баллард К., Фаркуар С. Эндометриоз. BMJ 2014;348:g1752. — пабмед
- Синаи Н.
 , Пламб К., Коттон Л., Ламберт А., Кеннеди С., Зондерван К. и др. Различия в характеристиках среди 1000 женщин с эндометриозом в зависимости от степени заболевания. Фертил Стерил 2008; 89: 538–45.
—
ЧВК
—
пабмед
, Пламб К., Коттон Л., Ламберт А., Кеннеди С., Зондерван К. и др. Различия в характеристиках среди 1000 женщин с эндометриозом в зависимости от степени заболевания. Фертил Стерил 2008; 89: 538–45.
—
ЧВК
—
пабмед
- Синаи Н.
- Верчеллини П., Вигано П., Сомильяна Э., Феделе Л. Эндометриоз: патогенез и лечение. Nat Rev Endocrinol 2014; 10: 261–75. — пабмед
- Somigliana E, Berlanda N, Benaglia L, Vigano P, Vercellini P, Fedele L.
 Хирургическое удаление эндометриом и резерв яичников: систематический обзор изменений уровня антимюллерова гормона в сыворотке. Фертил Стерил 2012; 98: 1531–8.
—
пабмед
Хирургическое удаление эндометриом и резерв яичников: систематический обзор изменений уровня антимюллерова гормона в сыворотке. Фертил Стерил 2012; 98: 1531–8.
—
пабмед
- Somigliana E, Berlanda N, Benaglia L, Vigano P, Vercellini P, Fedele L.
Типы публикаций
термины MeSH
Заместительная гормональная терапия у молодых женщин с хирургической первичной недостаточностью яичников
1. Asante A, Whiteman MK, Kulkarni A, Cox S, Marchbanks PA, Jamieson DJ. Плановая овариэктомия в США: тенденции и госпитальные осложнения, 1998–2006 гг. Акушерство Гинекол. 2010; 116:1088–1095. [PubMed: 20966693] [PubMed] [Google Scholar]
2. Wright JD, Herzog TJ, Tsui J, Ananth CV, Lewin SN, Lu YS, et al. Общенациональные тенденции выполнения гистерэктомии в США. Акушерство Гинекол. 2013; 122:233–41. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Акушерство Гинекол. 2013; 122:233–41. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Rebbeck TR, Kauff ND, Domcheck SM. Метаанализ оценок снижения риска, связанного со снижающей риск сальпингоовариэктомией у носителей мутации BRCA1 или BRCA2. J. Natl Cancer Inst. 2009; 191:80–87. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Gierach GL, Pfeiffer RM, Patel DA, Black A, Schairer C, Gill A. Долгосрочная общая и специфичная для заболевания смертность, связанная с доброкачественной гинекологической хирургией, выполненной в разном возрасте. Менопауза. 2014;21(6):592–601. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Shuster LT, Rhodes DJ, Gostout BS, Grosshardt BR, Rocca WA. Преждевременная менопауза или ранняя менопауза: долгосрочные последствия для здоровья. Зрелые. 2010;65:161–166. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Faubion SS, Kuhle CL, Shuster LT, Rocca WA. Долгосрочные последствия для здоровья преждевременной или ранней менопаузы и соображения по лечению. Климактерический. 2015;18(4):483–91. [PMC free article] [PubMed] [Google Scholar]
Климактерический. 2015;18(4):483–91. [PMC free article] [PubMed] [Google Scholar]
7. Чубатый А., Шандро М.Т., Шуурманс Н., Юксель Н. Практика гормональной терапии после хирургической менопаузы. Зрелые. 2011;69(1):69–73. [PubMed] [Google Scholar]
8. Беншушан А., Рожанский Н., Чавив М., Арбель-Алон С., Бенмеир А., Имбар Т. и соавт. Климактерические симптомы у женщин, перенесших двустороннюю сальпингоовариэктомию с целью снижения риска. Климактерический. 2009 г.;12:404–409. [PubMed] [Google Scholar]
9. Нахтигалл Л. Приливы: приливы — это просто приливы? Менопауза. 2014;2155(6):1–2. [PubMed] [Google Scholar]
10. Thurston RC, El Khoudary SR, Sutton-Tyrrell K, Crandall CJ, Gold E, Sternfeld B, et al. Связаны ли вазомоторные симптомы с изменениями гемостатических и воспалительных маркеров? Результаты исследования женского здоровья в стране. Менопауза. 2011;18:1044–1051. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Rossouw JE, Prentice RL, Manson JE, Wu L, Barad D, Barnabei VM, et al. Постменопаузальная гормональная терапия и риск сердечно-сосудистых заболеваний в зависимости от возраста и лет после менопаузы. ДЖАМА. 2007; 297:1465–1477. [PubMed] [Google Scholar]
Постменопаузальная гормональная терапия и риск сердечно-сосудистых заболеваний в зависимости от возраста и лет после менопаузы. ДЖАМА. 2007; 297:1465–1477. [PubMed] [Google Scholar]
12. Кроненберг Ф. Приливы, эпидемиология и физиология. Энн Н.Ю. Академия наук. 1990; 592: 122–133. [PubMed] [Google Scholar]
13. Challberg J, Ashcroft L, Lalloo F, Eckersley B, Clayton R, Hopwood P, et al. Симптомы менопаузы и здоровье костей у женщин, подвергающихся риску снижения двусторонней сальпингоовариэктомии: серьезные проблемы со здоровьем костей у тех, кто не принимает ЗГТ. Британский журнал рака. 2011;105:22–27. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Фридман Р.Р. Физиология приливов. Am J Hum Biol. 2001; 13: 453–464. [PubMed] [Google Scholar]
15. Sarrel PM, Lindsay DC, Rosano GMC, Poole-Wilson PA. Стенокардия и нормальные коронарные артерии у женщин: гинекологические данные. Am J Obstet Gynecol. 1992; 167: 467–472. [PubMed] [Google Scholar]
16. Sarrel PM. Сексуальность и менопауза. Акушерство Гинекол. 1990;75(прил.):26С–30С. [PubMed] [Google Scholar]
Sarrel PM. Сексуальность и менопауза. Акушерство Гинекол. 1990;75(прил.):26С–30С. [PubMed] [Google Scholar]
17. Thurston RC, Aizenstein HJ, Derby CA, Sejdic E, Maki PM. Менопаузальные приливы и гиперинтенсивность белого вещества. Менопауза. 2016;23(1):27–31. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Bove R, Secor E, Chibnik LB, Barnes LL, Schneider JA, Bennett DA, De Jager PL. Возраст хирургической менопаузы влияет на снижение когнитивных функций и патологию Альцгеймера у пожилых женщин. Неврология. 2014;82:222–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Sarrel PM, Portman D, Lefebvre MA, Lafeuille MH, Grittner AM, Fortier J, et al. Дополнительные прямые и косвенные затраты на нелеченные вазомоторные симптомы. Менопауза. 2015;22(3):260–66. [PubMed] [Google Scholar]
20. Geukes M, VanAalst MP, Rebroek SJW, Laven JSE, Oosterhof H. Влияние менопаузы на трудоспособность женщин с тяжелыми симптомами менопаузы. Зрелые. 2016;90:3–8. [PubMed] [Google Scholar]
21. Graziottin A, Basson R. Сексуальная дисфункция у женщин с преждевременной менопаузой. Менопауза. 2004; 11: 766–77. [PubMed] [Google Scholar]
Graziottin A, Basson R. Сексуальная дисфункция у женщин с преждевременной менопаузой. Менопауза. 2004; 11: 766–77. [PubMed] [Google Scholar]
22. Shifren JL, Braunstein GD, Simon JA, Casson PR, Buster JE, Redmond GP, et al. Трансдермальная терапия тестостероном у женщин с нарушением половой функции после овариэктомии. N Engl J Med. 2000;343(10):682–8. [PubMed] [Google Scholar]
23. Tucker PE, Bulsara MK, Salfinger SG, Tan JJ, Green H, Cohen PA. Влияние предоперационного менопаузального статуса и заместительной гормональной терапии (ЗГТ) на сексуальность и качество жизни после сальпингоофорэктомии, снижающей риск. Зрелые. 2016 март; 85: 42–8. [PubMed] [Академия Google]
24. Розенберг Л., Хеннекенс С.Х., Рознер Б., Беланже С., Ротман К.Дж., Спейзер Ф.Е. Ранняя менопауза и риск инфаркта миокарда. Am J Obstet Gynecol. 1981; 139: 47–51. [PubMed] [Google Scholar]
25. Thurston RC, Barinas-Mitchell E, Jennings JR, Santoro N, von Kanel R, Chang Y, et al. Физиологически контролируемые приливы и субклинические сердечно-сосудистые заболевания среди женщин среднего возраста. Менопауза. 2015;22:1371. [Google Scholar]
Менопауза. 2015;22:1371. [Google Scholar]
26. Кербер И.Дж., Тернер Р.Дж. Eu-эстрогенемия, нейроны KNDY и вазомоторные симптомы. JAMA Внутренняя медицина. 2015;175(9): 1586. [PubMed] [Google Scholar]
27. Hodis HN, Mack WJ. Гипотеза времени и заместительная гормональная терапия: изменение парадигмы в первичной профилактике ишемической болезни сердца у женщин. Части 1 и 2. J Am Geriatr Soc. 2013;61(6):1005–1018. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Carroll JS, Meyer CA, Song J, LI W, Geistlinger TR, Eeckhoute J, et al. Полногеномный анализ сайтов связывания рецепторов эстрогена. Генетика природы. 2006;38(11):1289–1297. [PubMed] [Академия Google]
29. Вуэст Дж. Х., Драй Т. Дж., Эдвардс Дж. Э. Степень коронарного атеросклероза у женщин с двусторонней оофорэктомией. Тираж. 1953; 7: 801–808. [PubMed] [Google Scholar]
30. Forte TF, редактор. Серия монографий Американской кардиологической ассоциации. Издательская компания Футура; Американская Ассоциация Сердца; Армонк, Нью-Йорк: 1997. Гормональное, метаболическое и клеточное влияние на сердечно-сосудистые заболевания у женщин. [Google Scholar]
Гормональное, метаболическое и клеточное влияние на сердечно-сосудистые заболевания у женщин. [Google Scholar]
31. Герхард М., Ганц П. Как объяснить клинические преимущества эстрогена? От кровати до скамейки. Тираж. 1995;92(1):5–8. [PubMed] [Google Scholar]
32. Lantto H, Mikkola TS, Tuomikoski P, Viitasalo M, Vaananen H, Sovijarvi ARA, et al. Сердечная реполяризация у женщин в недавно постменопаузальном периоде с приливами или без них. Менопауза. 2016;23(5):528–534. [PubMed] [Google Scholar]
33. Mikkola TS, Tuomikoski P, Lytinen H, Korhonen P, Hoti F, Vattulainen P, et al. Повышенный риск смертности от сердечно-сосудистых заболеваний у женщин, прекративших гормональную терапию в постменопаузе. J Clin Endocinol Metab. 2015;10:4588–94. [PubMed] [Google Scholar]
34. Allison MA, Manson JE, Langer RD, Carr JJ, Rossouw JE, Pettinger MB, et al. Оофорэктомия, гормональная терапия, субклиническая болезнь коронарных артерий у женщин с гистерэктомией: исследование кальция в коронарных артериях Инициативы женского здоровья. Менопауза. 2008; 15 (4 часть 1): 639–47. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Менопауза. 2008; 15 (4 часть 1): 639–47. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Harman SM, Black DM, Naftolin F, Brinton EA, Budoff MJ, Cedars MI, et al. Результаты визуализации артерий и факторы сердечно-сосудистого риска у женщин с недавно наступившей менопаузой: рандомизированное исследование. Энн Интерн Мед. 2014;161:249–60. [PubMed] [Google Scholar]
36. Hodis HN, Mack WJ, Henderson VW, Kono N, Stanczyk F, Selzer S, et al. Сосудистые эффекты лечения эстрадиолом в ранней и поздней постменопаузе. N Engl J Med. 2016; 374:1221–31. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Ингельссон Э., Лундхольм С., Йоханссон А.Л., Альтман Д. Гистерэктомия и риск сердечно-сосудистых заболеваний: популяционное когортное исследование. Европейское сердце J. 2011; 32 (6): 745–50. [PubMed] [Google Scholar]
38. Lokkegaard E, Jovanovic Z, Heitmann BL, Kelding N, Ottesen B, Pedersen AT. Связь между ранней менопаузой и риском ишемической болезни сердца: влияние гормональной терапии. Зрелые. 2006;53(2):226–33. [PubMed] [Академия Google]
Зрелые. 2006;53(2):226–33. [PubMed] [Академия Google]
39. Atsma F, Bartelink MEL, Grobbee DE, van der Schouw Y. Постменопаузальный статус и ранняя менопауза как независимые факторы риска сердечно-сосудистых заболеваний: метаанализ. Менопауза. 2006;13(2):265–279. [PubMed] [Google Scholar]
40. Carr MC. Возникновение метаболического синдрома при климаксе. J Clin Метабол эндокринолов. 2003; 88: 2404–2411. [PubMed] [Google Scholar]
41. Пиримоглу З.М., Арслан С., Буюкбайрак Э.Е., Карс Б., Карсидаг Ю.К., Унал О. и соавт. Толерантность к глюкозе у женщин в пременопаузе после менопаузы в связи с хирургическим удалением яичников. Климактерический. 2011; 14:453–457. [PubMed] [Академия Google]
42. Аппиа Д., Винтерс С.Дж., Хомунг, Калифорния. Двусторонняя овариэктомия и риск развития диабета у женщин в постменопаузе. Уход за диабетом. 2014;37:725–33. [PubMed] [Google Scholar]
43. Дорум А., Тонстад С., Лиавааг А.Х., Михельсен Т.М., Хильдрам Д., Даль А.А. Двусторонняя овариэктомия в возрасте до 50 лет в значительной степени связана с метаболическим синдромом и шкалой риска Framingham: контролируемое популяционное исследование (HUNT-2) Gynecol Oncol. 2008; 109: 377–383. [PubMed] [Академия Google]
2008; 109: 377–383. [PubMed] [Академия Google]
44. Kim C, Edelstein SL, Crandall JP, Diabelea D, Kitabchi AE, Hamman RF, et al. Исследовательская группа программы профилактики диабета. Менопауза и риск диабета в программе профилактики диабета. Менопауза. 2011;18:857–868. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Йошида Т., Такахаши К., Яматани Х., Таката К., Курачи Х. Влияние хирургической менопаузы на липидный и костный метаболизм. Климактерический. 2011; 14:445–452. [PubMed] [Google Scholar]
46. Линдси Р. Менопауза: половые стероиды и остеопороз. Клин Обстет Гинекол. 1987;30(4):847–859. [PubMed] [Google Scholar]
47. Mucowski SJ, Mack WJ, Shoupe D, Kono N, Paulson R, Hodis HN. Влияние предшествующей овариэктомии на изменения минеральной плотности кости и толщины комплекса интима-медиа сонных артерий у женщин в постменопаузе. Фертил Стерил. 2014;101(4):1117–1122. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. Rocca WA, Bower JH, Maraganore DM, Ahlskog JE, Grosshardt BR, deAndrade M, et al. Повышенный риск когнитивных нарушений или деменции у женщин, перенесших овариэктомию до наступления менопаузы. Неврология. 2007;69: 1074–83. [PubMed] [Google Scholar]
Повышенный риск когнитивных нарушений или деменции у женщин, перенесших овариэктомию до наступления менопаузы. Неврология. 2007;69: 1074–83. [PubMed] [Google Scholar]
49. Phung TK, Waltoft BL, Laursen TM, Settnes A, Kessing LV, Mortensen PB, Waldemar G. Гистерэктомия, удаление яичников и риск деменции: общенациональное историческое когортное исследование. Дементное гериатрическое когнитивное расстройство. 2010;30(1):43–50. [PubMed] [Google Scholar]
50. Shao H, Breitner JCS, Whitmer RA, Wang J, Hayden K, Wengreen H, et al. Гормональная терапия и болезнь Альцгеймера. Неврология. 2012;79(18):1846–52. [Бесплатная статья PMC] [PubMed] [Google Scholar]
51. Рокка В.А., Гроссхардт Б.Р., Шустер Л.Т. Оофорэктомия, эстроген и деменция: обновление 2104 года. Мол Селл Эндокринол. 2014; 389:7–12. [Бесплатная статья PMC] [PubMed] [Google Scholar]
52. Rocca WA, Grosshardt BR, Geda YE, Gostout BS, Bower JH, Maraganore DM, et al. Долгосрочный риск депрессивных и тревожных симптомов после ранней овариэктомии. Менопауза. 2008;15(6):1050–1059. [PubMed] [Google Scholar]
Менопауза. 2008;15(6):1050–1059. [PubMed] [Google Scholar]
53. Nathorst-Boos J, von Schoultz B, Carlstrom K. Избирательное удаление яичников и заместительная терапия эстрогенами — влияние на сексуальную жизнь, психологическое благополучие и андрогенный статус. J Psychosom Obstet Gynaecol. 1993;14:283–293. [PubMed] [Google Scholar]
54. Cohen LS, Soares CN, Vitonis AF, Otto MW, Harlow BL. Риск новой депрессии во время менопаузального перехода: Гарвардское исследование настроений и циклов. Арх генерал психиатрия. 2006;63(4):385–90. [PubMed] [Google Scholar]
55. Soares CN, Almeida OP, Joffe H, Cohen LS. Эффективность эстрадиола для лечения депрессивных расстройств у женщин в перименопаузе: двойное слепое рандомизированное плацебо-контролируемое исследование. Арх генерал психиатрия. 2001;58(6):529–34. [PubMed] [Google Scholar]
56. Zweifel JE, O’Brien WH. Метаанализ влияния заместительной гормональной терапии на депрессивное настроение. Психонейроэндокринология. 1997;22(3):189–212. [PubMed] [Google Scholar]
1997;22(3):189–212. [PubMed] [Google Scholar]
57. Gibson CJ, Joffe H, Bromberger JT, Thurston RC, Lewis TT, Khalil N, et al. Симптомы настроения после естественной менопаузы и гистерэктомии с двусторонней овариэктомией и без нее у женщин среднего возраста. Акушерство Гинекол. 2012; 119: 935–41. [Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Rivera CM, Grosshardt BR, Rhodes DJ, Brown RD, JR, Roger VL, Melton LJ, 3rd, et al. Повышенная сердечно-сосудистая смертность после ранней двусторонней овариэктомии. Менопауза. 2009;16(1):15–23. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. Parker WH, Feskanich D, Broder MS, Chang E, Shoupe D, Farquhar CM, et al. Долгосрочная смертность, связанная с овариэктомией, по сравнению с сохранением яичников в исследовании здоровья медсестер. Акушерство Гинекол. 2013; 121:709–16. [Бесплатная статья PMC] [PubMed] [Google Scholar]
60. Солпитер С.Р., Ченг Дж., Табане Л., Бакли Н.С., Солпитер Э.Е. Байесовский метаанализ гормональной терапии и смертности у молодых женщин в постменопаузе. Am J Med. 2009; 122:1016–1022. [PubMed] [Google Scholar]
Am J Med. 2009; 122:1016–1022. [PubMed] [Google Scholar]
61. Sarrel PM, Njike VY, Vinante V, Katz DL. Смертность от избегания эстрогена: анализ избыточных смертей среди женщин с гистерэктомией в возрасте от 50 до 59 лет. AJPH. 2013;103(9):1583–88. [Бесплатная статья PMC] [PubMed] [Google Scholar]
62. Chlebowski RT, Anderson GL. Изменение концепций: менопаузальная гормональная терапия и рак молочной железы. J Natl Cancer Inst. 2012; 104: 517–527. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. LaCroix AZ, Chlebowski RT, Manson JE, Aragaki AK, Johnson KC, Martin L, et al. Последствия для здоровья после прекращения приема конъюгированных лошадиных эстрогенов у женщин в постменопаузе с предшествующей гистерэктомией: рандомизированное контролируемое исследование. ДЖАМА. 2011;305(13):1305–1314. [Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Schierbeck LL, Rejnmark L, Tofteng CL, Stilgren L, Eiken P, Mosekilde L, et al. Влияние заместительной гормональной терапии на сердечно-сосудистые события у женщин в постменопаузе: рандомизированное исследование. БМЖ. 2012;345:e6409. [PubMed] [Google Scholar]
БМЖ. 2012;345:e6409. [PubMed] [Google Scholar]
65. Маркетти С., Ядарола Р., Палайя И., ди Донато В., Перниола Г., Музиль Л. и др. Гормональная терапия у носителей мутации BRCA 1/2 после овариэктомии. Менопауза. 2014;21(7):763–768. [PubMed] [Google Scholar]
66. Rebbeck TR, Friebel T, Wagner T, Lynch HT, Garber JE, Daly MB, et al. Влияние краткосрочной заместительной гормональной терапии на снижение риска рака молочной железы после двусторонней овариэктомии у носителей мутаций BRCA1 и BRCA2: исследовательская группа PROST. Дж. Клин Онкол. 2005;23(31):7804–10. [PubMed] [Академия Google]
67. Armstrong K, Schwartz JS, Randall T, Rubin SC, Weber B. Заместительная гормональная терапия и ожидаемая продолжительность жизни после профилактической овариэктомии у женщин с мутациями BRCA1/2: анализ решения. Дж. Клин Онкол. 2004;22(6):1045–54. [PubMed] [Google Scholar]
68. O’Brien KM, Fei C, Sandler DP, Nichols HB, DeRoo LA, Weinberg CR. Гормональная терапия и рак молочной железы в молодом возрасте. Am J Эпидемиол. 2015;181(10):799–807. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Am J Эпидемиол. 2015;181(10):799–807. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Parker W, Broder M, Chang E, Feskanich D, Farquhar C, Liu Z, et al. Сохранение яичников во время гистерэктомии и долгосрочные последствия для здоровья в исследовании здоровья медсестер. Акушерство Гинекол. 2009 г.;113(5):1027–1037. [Бесплатная статья PMC] [PubMed] [Google Scholar]
70. Бюллетени комитета ACOG по практике Выборочная и снижающая риск сальпингоовариэктомия. 2008 ACOG Practice Bulletin Number 89. [Google Scholar]
71. Moorman PG, Myers ER, Schildkraut JM, Iversen ES, Wand F, Warren N. Влияние гистерэктомии с сохранением яичников на функцию яичников. Акушер Гинек. 2011;118(6):1271–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
72. Trabuco EC, Moorman PG, Algeciras-Schimnich A, Weaver AL, Cliby WA. Ассоциация яичникосохраняющей гистерэктомии с овариальным резервом. Акушерство Гинекол. 2016;127:81, 9–827. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73.
